
Wetenschap
Wat is de elektronische structuur van zwavel?
* Atomisch nummer: 16
* Elektronische configuratie: 1S² 2S² 2P⁶ 3S² 3P⁴
Verklaring:
* 1S²: Het eerste energieniveau (n =1) heeft 2 elektronen in de 1s orbital.
* 2S²: Het tweede energieniveau (n =2) heeft 2 elektronen in de 2s orbital.
* 2p⁶: Het tweede energieniveau (n =2) heeft 6 elektronen in de 2p orbitalen (2px, 2py, 2pz).
* 3S²: Het derde energieniveau (n =3) heeft 2 elektronen in de 3s orbital.
* 3P⁴: Het derde energieniveau (n =3) heeft 4 elektronen in de 3P -orbitalen (3px, 3py, 3pz).
Visuele weergave:
U kunt dit elektronisch vertegenwoordigen met een orbitaal diagram:
`` `
1S 2S 2p 3s 3p
↑ ↓ ↑ ↓ ↑ ↓ ↑ ↓ ↑ ↓ ↑ ↓ ↑ ↓ ↑
`` `
Sleutelpunten:
* valentie -elektronen: Zwavel heeft 6 valentie -elektronen (de elektronen in het buitenste energieniveau, n =3). Dit zijn de elektronen die betrokken zijn bij chemische binding.
* Reactiviteit: De aanwezigheid van slechts 4 elektronen in de 3P -orbitalen maakt zwavelreactief, en probeert nog 2 elektronen te krijgen om een stabiele octetconfiguratie te bereiken.
Laat het me weten als je nog andere vragen hebt!
 Wat maken magnesium en zwavel?
Wat maken magnesium en zwavel?  Hoe sublimeren naftaleenballen?
Hoe sublimeren naftaleenballen?  Wanneer natriumatomen (Na) en chloor (Cl) samenkomen om chloride of keukenzout te maken, vormen ze een ionische binding. Gebruikmakend van deze informatie, welk paar elementen is waarschijnlijk een binding?
Wanneer natriumatomen (Na) en chloor (Cl) samenkomen om chloride of keukenzout te maken, vormen ze een ionische binding. Gebruikmakend van deze informatie, welk paar elementen is waarschijnlijk een binding?  Wat is een voorbeeld van heterogene -mengsel?
Wat is een voorbeeld van heterogene -mengsel?  Waar staat F en C voor op een thermonater?
Waar staat F en C voor op een thermonater?
Hoofdlijnen
- Hoe we een opmerkelijke vlucht van een kleine zeevogelsoort naar een tyfoon hebben gevolgd
- Wat zijn de eiwitten ingebed in lipide dubbellaag?
- Wat is de oorsprong van frank?
- Plastic voor het avondeten? Grote vissen eten meer dan je verwacht
- Wat betekent piocytaire?
- Waarom zijn sommige bacteriën grampositief en gram-negatief?
- Wat is waarneembaar door wetenschappelijke methoden in de psychologie?
- Netwerkassemblage door celdeling:hoe zenuwcellen in de hersenen verbinding maken tijdens de ontwikkeling
- Neanderthalers hadden grotere hersenen dan moderne mensen - waarom zijn we slimmer?
- Plantenonderzoekers onderzoeken broodaroma:moderne en oude tarwesoorten smaken even goed

- Onderschatte chemische diversiteit

- Op zoek naar een behandeling voor IBS-pijn in tarantulagif

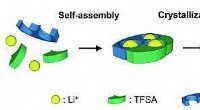
- Vaste kristallen die zichzelf assembleren om kanalen voor een elektrische stroom te vormen, kunnen veiligere batterijen maken
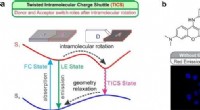
- Onderzoekers ontdekken nieuw proces voor ladingsoverdracht en scheiding
 Een stap dichter bij praktische zonne-waterstofproductie via uitgebreid gemodificeerde hematiet-fotoanode
Een stap dichter bij praktische zonne-waterstofproductie via uitgebreid gemodificeerde hematiet-fotoanode Wat kan waterdamp condenseren?
Wat kan waterdamp condenseren?  Hoe levert perfluoroctylbromide zuurstof aan weefsels?
Hoe levert perfluoroctylbromide zuurstof aan weefsels?  Qatar tekent zonne-deal van $ 470 miljoen
Qatar tekent zonne-deal van $ 470 miljoen De gemiddelde dikte van de korst is?
De gemiddelde dikte van de korst is?  Voorschoolse ouders maken zich zorgen dat hun kinderen cruciale sociale vaardigheden mislopen tijdens de pandemie
Voorschoolse ouders maken zich zorgen dat hun kinderen cruciale sociale vaardigheden mislopen tijdens de pandemie Wat is het volume van één nanocontainer?
Wat is het volume van één nanocontainer?  Wat is SR en RB in geologische isochron?
Wat is SR en RB in geologische isochron?
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

