
Wetenschap
Hoe reageert waterstofgas met zwavel?
Hier is de evenwichtige chemische vergelijking:
h₂ (g) + s (s) → h₂s (g)
Hier is een uitsplitsing van de reactie:
* waterstofgas is een diatomee molecuul bestaande uit twee aan elkaar verbonden waterstofatomen.
* zwavel is een vast element bij kamertemperatuur.
* waterstofsulfide is een gas met een sterke, scherpe geur. Het is zeer giftig en brandbaar.
De reactie wordt meestal uitgevoerd in een gesloten container, omdat waterstofsulfide een vluchtig en potentieel gevaarlijk gas is.
Opmerking: De reactie tussen waterstof en zwavel kan ook andere verbindingen produceren, zoals polysulfiden (H₂Sₓ), afhankelijk van de reactieomstandigheden. Het primaire product is echter waterstofsulfide.
 Hoeveel mol NH3 ontstaat er als 1,4 H2 reageert?
Hoeveel mol NH3 ontstaat er als 1,4 H2 reageert?  Nieuwe toepassingen vinden voor afvalbanden
Nieuwe toepassingen vinden voor afvalbanden Wat is de evenwichtige vergelijking als natrium reageert met water om hydroxide en waterstof te vormen?
Wat is de evenwichtige vergelijking als natrium reageert met water om hydroxide en waterstof te vormen?  Waarom heeft calciumfluoride een hoger smeltpunt dan chloorfluoride?
Waarom heeft calciumfluoride een hoger smeltpunt dan chloorfluoride?  Het barsten van oliedruppels onder water:hoe vervuiling in het water kan achterblijven na het opruimen van lekkages
Het barsten van oliedruppels onder water:hoe vervuiling in het water kan achterblijven na het opruimen van lekkages
Hoofdlijnen
- Waarom worden planten geclassificeerd als levende wezens?
- Wat was de bijdrage aan de celtheorie?
- Onder levende wezens is de meest voorkomende onder polysaccharide structurele koolhydraten?
- Hoe wordt plagioklaas gebruikt?
- Zijn alle symbiotische organismen onschadelijk voor mensen?
- Hoe erfelijke ziekten werken
- Vergeet haaien... dit is de reden waarom je meer kans loopt gewond te raken door zwerfvuil op het strand
- Wetenschappers tonen een moleculaire basis aan voor mieren die fungeren als 'lijfwachten'-planten
- Wat is de Rhinoceros Beetle Scientific Name?
- Een biomassa-naar-vloeistoffabriek voor de productie van duurzame synthetische brandstof

- Wetenschappers ontwikkelen op papier gebaseerde sensoren voor koolstofdioxide

- Kleine pomp bouwt polyrotaxanen met precisie
- Door de bodem kijken kan boeren helpen om toekomstige droogtes het hoofd te bieden

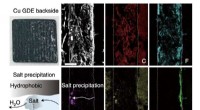
- Bifunctionele ionomeren gebruiken als elektrolyten om ethyleen uit koolstofdioxide te synthetiseren
 Werken om nieuwe behandelingen voor tuberculose te ontdekken
Werken om nieuwe behandelingen voor tuberculose te ontdekken Studie:zelfs kortlevende zonnepanelen kunnen economisch levensvatbaar zijn
Studie:zelfs kortlevende zonnepanelen kunnen economisch levensvatbaar zijn Wetenschappers leren meer over hoe motoren de wegen van onze cellen manoeuvreren
Wetenschappers leren meer over hoe motoren de wegen van onze cellen manoeuvreren  Tijdens een chemische of fysieke verandering kan energie zijn?
Tijdens een chemische of fysieke verandering kan energie zijn?  China waarschuwt de VS voor het bewapenen van de ruimte
China waarschuwt de VS voor het bewapenen van de ruimte Wat is de taak van de celwand, welk deel van een plantencel?
Wat is de taak van de celwand, welk deel van een plantencel?  Wat is een dubbele vervangingsreactie?
Wat is een dubbele vervangingsreactie?  In een eerste, wetenschappers vangen een kwantumsleepboot tussen naburige watermoleculen
In een eerste, wetenschappers vangen een kwantumsleepboot tussen naburige watermoleculen
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

