
Wetenschap
In welke wet stelt dat als twee of meer verbindingen bestaan uit dezelfde elementen van de elementen Ratio Masses Second Element is altijd een kleine hele getallen?
Hier is een meer gedetailleerde uitleg:
Wet van meerdere verhoudingen
Deze wet stelt dat wanneer twee elementen combineren om meer dan één verbinding te vormen, de massa's van het ene element dat combineert met een vaste massa van het andere element bevinden zich in een eenvoudige ratio van het hele nummer.
Voorbeeld:
* Beschouw de verbindingen koolmonoxide (CO) en koolstofdioxide (CO₂).
* Beide verbindingen bestaan uit koolstof en zuurstof.
* In CO is de massaverhouding van koolstof en zuurstof 12:16 (ongeveer).
* In CO₂ is de massaverhouding van koolstof en zuurstof 12:32 (ongeveer).
* Merk op dat de massa zuurstof die combineert met een vaste massa koolstof (12) in CO₂ tweemaal de massa zuurstof is die combineert met dezelfde koolstofmassa in co.
* Deze verhouding van 1:2 is een eenvoudige ratio van het hele nummer, zoals vermeld door de wet van meerdere verhoudingen.
Sleutelpunten:
* Deze wet helpt het bestaan van meerdere verbindingen uit dezelfde elementen te verklaren.
* Het levert bewijs voor het bestaan van atomen en het idee dat atomen combineren in vaste verhoudingen om moleculen te vormen.
* Deze wet werd door John Dalton voorgesteld als onderdeel van zijn atoomtheorie.
Laat het me weten als je nog vragen hebt!
 Uit onderzoek blijkt hoe afval kan worden omgezet in materialen voor geavanceerde industrieën
Uit onderzoek blijkt hoe afval kan worden omgezet in materialen voor geavanceerde industrieën  Cellulaire schoonmaakploegen gekoppeld aan hoe het lichaam met suiker omgaat
Cellulaire schoonmaakploegen gekoppeld aan hoe het lichaam met suiker omgaat Eénpotstrategie om tegelijkertijd heterodehydrokoppeling van hydrostannaan en reductie van chinoline te bereiken
Eénpotstrategie om tegelijkertijd heterodehydrokoppeling van hydrostannaan en reductie van chinoline te bereiken  Wat is het verschil tussen spachloor en zwembadchloor?
Wat is het verschil tussen spachloor en zwembadchloor?  Vaste zwavel (32 g/mol) pH =7,16 pH in ppm?
Vaste zwavel (32 g/mol) pH =7,16 pH in ppm?
 Het koppelen van bladelementaire eigenschappen aan biomassa in bosbiomen in de Himalaya
Het koppelen van bladelementaire eigenschappen aan biomassa in bosbiomen in de Himalaya  Rook van Amerikaanse branden bereikt Europa, satellietgegevens laten zien
Rook van Amerikaanse branden bereikt Europa, satellietgegevens laten zien Afbeelding:branden in Botswana
Afbeelding:branden in Botswana Afnemend Arctisch zee-ijs beïnvloedt het Europese weer, maar is geen oorzaak van koudere winters
Afnemend Arctisch zee-ijs beïnvloedt het Europese weer, maar is geen oorzaak van koudere winters NASA vindt dat de regenval afneemt in een verzwakkende tropische storm Eugene
NASA vindt dat de regenval afneemt in een verzwakkende tropische storm Eugene
Hoofdlijnen
- Om de hypothese te testen, moet een wetenschapper?
- Ben je Facebook-afhankelijk?
- Waar komen stamcellen vandaan?
- Welk dier behoort tot de klasse Oligochaeta?
- Hoe wordt het DNA opgeroepen?
- Wat is 11Degease Celleneas in Fahrenheit?
- Hoe transcriptiefactoren het genoom verkennen
- Wat heeft wetenschapper Robert Whittaker Develope?
- Zijn er dieren immuun voor prionziekten?
- Materiaalwetenschappers creëren stoffen alternatief voor batterijen voor draagbare apparaten

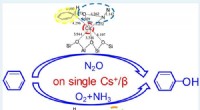
- Verbeterde katalytische processen voor de synthese van fenol
- Video:kleine vormveranderende polymeren ontwikkeld voor potentiële medische toepassingen

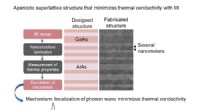
- Minimaliseren van thermische geleidbaarheid van kristallijn materiaal met optimale nanostructuur
- Gels gemaakt van druppeltjes zijn minder stabiel dan gels gemaakt van vaste deeltjes

 Nieuwe details over hoe een viraal eiwit de replicatie van virussen remt
Nieuwe details over hoe een viraal eiwit de replicatie van virussen remt  Welke wetenschapper zag het atoom als een bal van postieve lading met elektronen die erin zijn ingebed?
Welke wetenschapper zag het atoom als een bal van postieve lading met elektronen die erin zijn ingebed?  Geofysicus:gewicht van Harvey-regens deed Houston zinken
Geofysicus:gewicht van Harvey-regens deed Houston zinken Biophotonics:in situ vloeibare superlenzen printen om vlindervleugels en nanobiostructuren in beeld te brengen
Biophotonics:in situ vloeibare superlenzen printen om vlindervleugels en nanobiostructuren in beeld te brengen Lijst met insecten met onvolledige metamorfose
Lijst met insecten met onvolledige metamorfose  Wat straalt licht uit met warmte?
Wat straalt licht uit met warmte?  in silicium, in leven, in-vitro-aanpak opent deuren voor op nanodeeltjes gebaseerde medicijnontdekking
in silicium, in leven, in-vitro-aanpak opent deuren voor op nanodeeltjes gebaseerde medicijnontdekking Wanneer lijkt de maan donker?
Wanneer lijkt de maan donker?
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

