
Wetenschap
Leg de deeltjesopstelling uit in vaste stoffen vloeistoffen en gassen Energy geassocieerd met elke fase?
deeltjesopstelling en energie in vaste stoffen, vloeistoffen en gassen
De toestanden van materie (vaste, vloeistof en gas) worden bepaald door de opstelling en beweging van hun samenstellende deeltjes (atomen, moleculen of ionen).
Hier is een uitsplitsing van hun eigenschappen:
vaste stoffen:
* arrangement: Deeltjes zijn strak verpakt en gerangschikt in een regelmatig, herhaaldelijk patroon dat een kristalrooster wordt genoemd.
* Beweging: Deeltjes trillen in vaste posities in het rooster. Ze hebben lage kinetische energie.
* energie: Vaste stoffen hebben de laagste energieniveaus van de drie staten.
* kenmerken: Vaste stoffen hebben een vaste vorm en volume. Ze zijn niet samendrukbaar en rigide.
vloeistoffen:
* arrangement: Deeltjes zijn dicht bij elkaar, maar zijn niet in een vaste opstelling. Ze hebben een meer ongeordende structuur in vergelijking met vaste stoffen.
* Beweging: Deeltjes kunnen langs elkaar bewegen, maar worden nog steeds tot elkaar aangetrokken. Ze hebben matige kinetische energie.
* energie: Vloeistoffen hebben hogere energieniveaus dan vaste stoffen maar lager dan gassen.
* kenmerken: Vloeistoffen hebben een vast volume maar nemen de vorm van hun container. Ze zijn relatief niet te samendrukbaar.
gassen:
* arrangement: Deeltjes zijn wijd verdeeld en zijn in constante, willekeurige beweging. Ze hebben geen vaste regeling.
* Beweging: Deeltjes bewegen vrij en onafhankelijk, botsen tegen elkaar en de wanden van hun container. Ze hebben de hoogste kinetische energie.
* energie: Gassen hebben de hoogste energieniveaus van de drie staten.
* kenmerken: Gassen hebben geen vaste vorm of volume. Ze zijn gemakkelijk samendrukbaar en breiden uit om hun container te vullen.
Energie- en fase -overgangen:
De energie geassocieerd met elke toestand is direct gerelateerd aan de kinetische energie van de deeltjes. Wanneer een stof energie (warmte) absorbeert, bewegen de deeltjes sneller en verhogen ze hun kinetische energie. Dit kan leiden tot een fase -overgang:
* Solid to Liquid (smelten): Het toevoegen van warmte verhoogt de kinetische energie van deeltjes in een vaste stof, waardoor ze loskomen van het starre rooster en vrijer bewegen. Dit resulteert in een vloeistof.
* vloeistof tot gas (koken/verdamping): Verdere verwarming verhoogt de kinetische energie, waardoor deeltjes in een vloeistof de aantrekkelijke krachten kunnen overwinnen die ze bij elkaar houden en ontsnappen in de gasvormige toestand.
* Gas tot vloeistof (condensatie): Wanneer gasdeeltjes energie verliezen, vertragen ze en worden ze dichter bij elkaar en vormen ze uiteindelijk een vloeistof.
* vloeistof tot vast (bevriezen): Het afkoelen van een vloeistof verwijdert energie, waardoor deeltjes vertragen en een rigide roosterstructuur vormen.
Belangrijke punten om te onthouden:
* Temperatuur is een maat voor de gemiddelde kinetische energie van deeltjes.
* Hoe hoger het energieniveau, hoe meer bewegingsvrijheid deeltjes hebben.
* Fasovergangen omvatten veranderingen in het energieniveau en de opstelling van deeltjes.
Door de relatie tussen deeltjesopstelling, beweging en energie te begrijpen, kunnen we de eigenschappen en het gedrag van verschillende toestanden van materie beter begrijpen.
 nasa, Nieuw-Zeelandse partner om klimaatgegevens van commerciële vliegtuigen te verzamelen
nasa, Nieuw-Zeelandse partner om klimaatgegevens van commerciële vliegtuigen te verzamelen Hoe de mens naar de aarde kwam?
Hoe de mens naar de aarde kwam?  Wat is een nat en warm klimaat aan de randen van tropen?
Wat is een nat en warm klimaat aan de randen van tropen?  Hoe beïnvloedt een aardbeving de culturele omgeving?
Hoe beïnvloedt een aardbeving de culturele omgeving?  Nieuwe tests kunnen kleine maar giftige deeltjes koolas in de bodem detecteren
Nieuwe tests kunnen kleine maar giftige deeltjes koolas in de bodem detecteren
Hoofdlijnen
- Wat is late telofase?
- Hoe cellen leren 'tellen'
- Bacteriecellen reproduceren aseksueel door wat?
- Een schimmel die brood opstrijdt, wordt gebeld?
- Zien is geloven:wetenschappers onthullen connectoom van het visuele systeem van de fruitvlieg
- Moderne celtheorie
- Hepatitis D:Hoe het virus van dieren op mensen overging
- Uit onderzoek van zeeotter blijkt dat het gebruik van gereedschap toegang geeft tot grotere prooien en tandschade vermindert
- Organismen met aanpassingen om te strijden om beperkte middelen kunnen overleven en hun genen nakomelingen doorgeven?
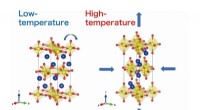
- Studie onderzoekt opmerkelijke negatieve thermische uitzetting gezien in gelaagde ruthenaten
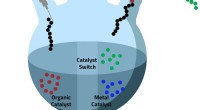
- Katalysatoromschakeling betekent dat vier één worden
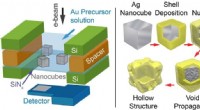
- Realtime beeldvorming van chemische processen
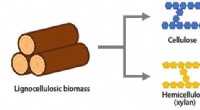
- Nieuwe strategie voor metabolische engineering verbetert de bioproductie van polymere grondstoffen
- Nieuwe studie verklaart de creatie van gels die pesticiden en andere stoffen op een gecontroleerde manier afgeven

 Luchtdichtheid tijdens de vlucht voorspellen voor een nauwkeurigere landing
Luchtdichtheid tijdens de vlucht voorspellen voor een nauwkeurigere landing Onderzoek:gemeenschapspolitie die het opbouwen van relaties aanmoedigt, kan politiegeweld verminderen
Onderzoek:gemeenschapspolitie die het opbouwen van relaties aanmoedigt, kan politiegeweld verminderen Reusachtige 200 jaar oude cactus omgevallen door hevige regen in de VS
Reusachtige 200 jaar oude cactus omgevallen door hevige regen in de VS Diagnose van ziekten in realtime met smartphones
Diagnose van ziekten in realtime met smartphones De waterstofproductie versnellen door de magische topologische oppervlaktetoestanden
De waterstofproductie versnellen door de magische topologische oppervlaktetoestanden Natuurkundigen tonen aan dat interacties tussen rook en wolken een onverwacht verkoelend effect hebben
Natuurkundigen tonen aan dat interacties tussen rook en wolken een onverwacht verkoelend effect hebben Wat leren kinderen in de astronomieklasse?
Wat leren kinderen in de astronomieklasse?  Hoe beïnvloedt de evolutie door natuurlijke selectie de biodiversiteit van het leven op aarde?
Hoe beïnvloedt de evolutie door natuurlijke selectie de biodiversiteit van het leven op aarde?
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

