
Wetenschap
Hoeveel moleculen zijn er in 3,5 gram H2O?
Hier leest u hoe u het aantal moleculen in 3,5 gram H₂o kunt berekenen:
1. Vind de molaire massa van H₂o:
* H:1,01 g/mol (x 2 =2,02 g/mol)
* O:16.00 g/mol
* Totaal:18,02 g/mol
2. Converteer grams naar mollen:
* Mol =(gram) / (molaire massa)
* Mol =3,5 g / 18,02 g / mol
* Mol ≈ 0,194 mol
3. Gebruik het nummer van Avogadro om het aantal moleculen te vinden:
* Avogadro's nummer:6.022 x 10²³ Moleculen/mol
* Aantal moleculen =(mol) x (Avogadro's nummer)
* Aantal moleculen ≈ 0,194 mol x 6,022 x 10²³ Moleculen/mol
* Aantal moleculen ≈ 1,17 x 10²³ Moleculen
Daarom zijn er ongeveer 1,17 x 10²³ watermoleculen in 3,5 gram H₂o.
 Hoeveel koolstof kan het land opnemen met meer koolstofdioxide in de atmosfeer?
Hoeveel koolstof kan het land opnemen met meer koolstofdioxide in de atmosfeer? Hoe bosbranden en het weer de Portugese volksgezondheid beïnvloeden
Hoe bosbranden en het weer de Portugese volksgezondheid beïnvloeden  Land en alle aan de natuurlijke door de mens gemaakte elementen die eraan zijn bevestigd, worden vaak aangeduid als?
Land en alle aan de natuurlijke door de mens gemaakte elementen die eraan zijn bevestigd, worden vaak aangeduid als?  Waar kan materie worden gevonden?
Waar kan materie worden gevonden?  Smartphones kunnen worden gebruikt om het weer beter te voorspellen
Smartphones kunnen worden gebruikt om het weer beter te voorspellen
Hoofdlijnen
- Hoe noem je de fysieke locatie van een gen?
- De verzorgingsgewoonten van apen geven aanwijzingen over hoe we met elkaar omgaan
- Hoe goede darmbacteriën het risico op hartziekten helpen verminderen
- Wat is de valentie van suiker?
- Hoe cellen kunstmatige ingrediënten 'lezen' die in een genetisch recept worden gegooid
- Wat is eiwitvrij filtraat?
- Wat maakt deel uit van het uitscheidingssysteem Annelids?
- Kunnen tweelingen elkaar voelen?
- Hoe verschillen schimmelsporen van bacteriële endosporen?
- Nieuw inzicht in celmembranen kan het testen en ontwerpen van geneesmiddelen verbeteren
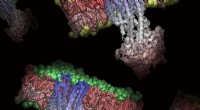
- Herstellen van actief pompend hartweefsel met op mosselen geïnspireerde weefsellijm

- Transparant hout kan warmte opslaan en afgeven

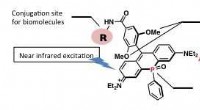
- Een nabij-infrarood fluorescerende kleurstof voor bio-imaging op lange termijn
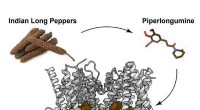
- Ingrediënt in Indiase lange peper veelbelovend tegen hersenkanker in diermodellen
 De chemie van de aarde modelleren:het onzichtbare zichtbaar maken
De chemie van de aarde modelleren:het onzichtbare zichtbaar maken Ruimtetelescopen gouden spiegelvleugels openen nog een laatste keer op aarde
Ruimtetelescopen gouden spiegelvleugels openen nog een laatste keer op aarde Timelapse toont vijfentwintig jaar uit het leven van een van de meest bestudeerde objecten in de astronomie:Supernova 1987a
Timelapse toont vijfentwintig jaar uit het leven van een van de meest bestudeerde objecten in de astronomie:Supernova 1987a Waarom Canada zijn netto-nul-belofte om de CO2-uitstoot te verminderen moet laten vallen?
Waarom Canada zijn netto-nul-belofte om de CO2-uitstoot te verminderen moet laten vallen? Hoe is het verspreiden van de zeebodem anders dan continentale drift?
Hoe is het verspreiden van de zeebodem anders dan continentale drift?  CHESS-röntgenfoto's laten zien hoe je kristallen uit kristallen kunt laten groeien
CHESS-röntgenfoto's laten zien hoe je kristallen uit kristallen kunt laten groeien Waarom hebben zure stoffen een lagere pH-waarde dan basische stoffen?
Waarom hebben zure stoffen een lagere pH-waarde dan basische stoffen?  Welke van deze termen kan worden gedefinieerd als een neerwaartse groeireactie op de zwaartekracht?
Welke van deze termen kan worden gedefinieerd als een neerwaartse groeireactie op de zwaartekracht?
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

