
Wetenschap
Waarom vormt SI geen dubbele binding met zuurstof?
* Grootte en elektronegativiteit: Silicium is groter en minder elektronegatief dan koolstof. Dit betekent dat de valentie -elektronen verder weg zijn van de kern en minder strak vastgehouden. Zuurstof, kleiner en meer elektronegatief, trekt de elektronen naar zich toe, waardoor het voor silicium moeilijker is om zijn elektronen in een dubbele binding te delen.
* π-binding: Dubbele obligaties omvatten de vorming van een Sigma -binding en een PI -binding. De PI-binding wordt gevormd door de zijwaartse overlapping van p-orbitalen. Silicium heeft een grotere atoomradius en de p-orbitalen zijn minder effectief in het vormen van sterke π-bindingen.
* D-orbitale participatie: Hoewel silicium lege D-orbitalen heeft, zijn ze niet direct beschikbaar voor binding vanwege hun hogere energieniveau. Hoewel sommige theorieën duiden op D-orbitale betrokkenheid bij π-binding, wordt het over het algemeen als minder significant beschouwd in vergelijking met de andere factoren.
gevolgen:
* siliciumdioxide (SiO2): Siliciumdioxide vormt een sterke covalente netwerkstructuur met enkele bindingen tussen silicium en zuurstof. Deze netwerkstructuur geeft siliciumdioxide het hoge smeltpunt en de hardheid.
* Siliconen: In plaats van dubbele bindingen te vormen met zuurstof, vormt silicium enkele bindingen met zuurstof en ook bindingen met organische groepen. Dit resulteert in de vorming van siliconen, die worden gebruikt in een breed scala van toepassingen vanwege hun unieke eigenschappen.
Samenvattend voorkomt de combinatie van siliconengrootte, elektronegativiteit en de moeilijkheid bij het vormen van stabiele π-bindingen om dubbele bindingen met zuurstof te vormen.
 Wat is nitraatzuur?
Wat is nitraatzuur?  Een stap dichter bij een waterstofeconomie met een efficiënte anode voor het splitsen van water
Een stap dichter bij een waterstofeconomie met een efficiënte anode voor het splitsen van water Wat is de coëfficiënt voor zuurstof in de gebalanceerde chemische vergelijkingsverbranding van heptantie C7H16?
Wat is de coëfficiënt voor zuurstof in de gebalanceerde chemische vergelijkingsverbranding van heptantie C7H16?  Kun je peroxide op een brandwond gebruiken om deze schoon te maken?
Kun je peroxide op een brandwond gebruiken om deze schoon te maken?  Hoeveel verbindingen kunnen koolstof en zuurstof vormen?
Hoeveel verbindingen kunnen koolstof en zuurstof vormen?
 Schrikkel een tweede 2016:waarom deze oudejaarsavond een extra seconde krijgt
Schrikkel een tweede 2016:waarom deze oudejaarsavond een extra seconde krijgt Mariene reservaten zijn van vitaal belang, maar staan onder druk
Mariene reservaten zijn van vitaal belang, maar staan onder druk Een stijging van 50% van het kooldioxidegehalte zou de regenval in de Amazone meer kunnen verminderen dan ontbossing
Een stijging van 50% van het kooldioxidegehalte zou de regenval in de Amazone meer kunnen verminderen dan ontbossing Gids voor tropische regenwouden:hoe regenwouden werken
Gids voor tropische regenwouden:hoe regenwouden werken  Waterstof is een van de toekomstige bestuurders van stookolie en milieuactivisten kunnen beide steunen
Waterstof is een van de toekomstige bestuurders van stookolie en milieuactivisten kunnen beide steunen
Hoofdlijnen
- Wat betekent homozygoot?
- Wat is de kleinste overervingseenheid?
- Is de menselijke soort hetzelfde als de mensheid?
- Waarom vluchtspiercellen in insecten duizenden mitochondriën bevatten?
- Welk instrument zou je gebruiken als je in de biologieklasse was en de kern van een wangcel wilde observeren?
- Je wandeling is zo duidelijk dat het diepe persoonlijkheidskenmerken kan onthullen
- Mensen gebruiken niet zoveel denkkracht als we graag denken
- Is een hoorn des overvloeds homogeen of heterogeen?
- Wat is productie in de wetenschap?
- Van polymeer afgeleide koolstof als metaalvrij, groen alternatief voor katalysatoren en nanokoolstoffen
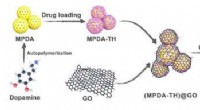
- Op cellulose-nanofibril gebaseerde inkapselingsstructuur om de afgifte van geneesmiddelen te regelen
- Een nieuw ontwerp voor flowbatterijen

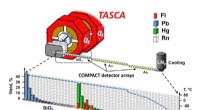
- Onderzoek toont aan dat flerovium het meest vluchtige metaal is in het periodiek systeem
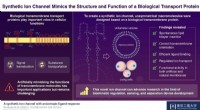
- Wetenschappers synthetiseren nieuwe kunstmatige moleculen die een celmembraaneiwit nabootsen
 Wat is de definitie van astroable?
Wat is de definitie van astroable?  Grote Meren krijgen extra geld voor opruimacties, invasieve soorten
Grote Meren krijgen extra geld voor opruimacties, invasieve soorten Het grootste dinosaurusskelet van Europa is mogelijk gevonden in Portugal
Het grootste dinosaurusskelet van Europa is mogelijk gevonden in Portugal Onderzoek met kleine bellen kan de hulpmiddelen van tandartsen verbeteren
Onderzoek met kleine bellen kan de hulpmiddelen van tandartsen verbeteren Tijdens welk proces vormen gassen de oplossing die u ademt?
Tijdens welk proces vormen gassen de oplossing die u ademt?  Welke vorm van energie veroorzaakt inefficiëntie bij de overdracht?
Welke vorm van energie veroorzaakt inefficiëntie bij de overdracht?  Nieuwe mastodontsoort ontdekt in Californië
Nieuwe mastodontsoort ontdekt in Californië Welke laag creëerde Earths Magnetic Field?
Welke laag creëerde Earths Magnetic Field?
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

