
Wetenschap
Wat is het verschil tussen elektronegativiteit van koolstof en zwavel?
Dit betekent dat zwavel iets meer elektronegatief is dan koolstof, maar het verschil is erg klein.
Elektronegativiteit is een maat voor het vermogen van een atoom om elektronen in een binding aan te trekken. Hoe hoger de elektronegativiteit, hoe sterker de aantrekkingskracht.
Hoewel het verschil tussen koolstof en zwavel gering is, kan het nog steeds invloed hebben op de eigenschappen van moleculen die deze elementen bevatten. Bij bijvoorbeeld koolstofdisulfide (CS₂) zijn de zwavelatomen iets meer elektronegatief, wat leidt tot een polaire binding. Deze polariteit beïnvloedt de algemene eigenschappen van het molecuul, zoals zijn kookpunt en oplosbaarheid.
 Snelle detectie van uraniumisotopen helpt bij het beschermen van nucleair materiaal
Snelle detectie van uraniumisotopen helpt bij het beschermen van nucleair materiaal Onderzoekers rapporteren strategie om te voorkomen dat de miltvuurbacterie ijzer absorbeert
Onderzoekers rapporteren strategie om te voorkomen dat de miltvuurbacterie ijzer absorbeert Wat zijn de reactanten en producten van een brandstof?
Wat zijn de reactanten en producten van een brandstof?  Welke opgeloste stof verhoogt het kookpunt van water het meest?
Welke opgeloste stof verhoogt het kookpunt van water het meest?  Wat zijn de functies van zout?
Wat zijn de functies van zout?
Hoofdlijnen
- Wat zijn enkele fysieke aanpassingen voor een kraai?
- Wat leidt er af. Wetenschap?
- Geen designerbaby’s, maar genbewerking om ziekten te voorkomen? Misschien
- Onderzoekers ontdekken hoe een klein molecuul de sleutel is tot HIV-vormende capsules
- Bevindingen van schimmels laten zien hoe celpunten hun weg banen
- Darmbacteriën vertellen de hersenen wat dieren moeten eten
- Hoe interageren de 3 componenten van de celtheorie met elkaar?
- Wetenschappers laten zien hoe eiwitten de evolutionaire inzet verslaan
- rRNA: Wat is het?
- AI-agent helpt materiaaleigenschappen sneller te identificeren

- Onderzoekers voorspellen falen in ongeordende materialen
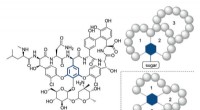
- Eenvoudige éénpotssynthese van medicamenteuze tricyclische peptiden
- Gebrouwen koffiedik biedt duurzaam alternatief voor kledingverf

- Gelijktijdige emissie van orthogonale handigheid in circulaire polarisatie

 Wat is een voorbeeld van B2G?
Wat is een voorbeeld van B2G?  Soorten Breezes
Soorten Breezes Poging om zwart gat in beeld te brengen, een kans om over Einstein te heersen
Poging om zwart gat in beeld te brengen, een kans om over Einstein te heersen Voetafdrukken gebruiken om reuzenpanda's in het wild te identificeren en te volgen
Voetafdrukken gebruiken om reuzenpanda's in het wild te identificeren en te volgen Licht beperken voor gebruik in nanofotonische apparaten
Licht beperken voor gebruik in nanofotonische apparaten Monitoring op afstand zou het gebruik van op de natuur gebaseerde oplossingen kunnen stimuleren om te beschermen tegen natuurlijke gevaren
Monitoring op afstand zou het gebruik van op de natuur gebaseerde oplossingen kunnen stimuleren om te beschermen tegen natuurlijke gevaren Wat is een breker als het gaat om golven?
Wat is een breker als het gaat om golven?  Nieuwe procedure zal de behoefte aan zeldzame metalen in chemische synthese verminderen
Nieuwe procedure zal de behoefte aan zeldzame metalen in chemische synthese verminderen
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

