
Wetenschap
Hoeveel moleculen water zijn er in water van 18 gram?
Hier leest u hoe u het aantal watermoleculen in 18 gram water kunt berekenen:
1. Vind de molaire watermassa (H₂o):
* Waterstof (H) heeft een molaire massa van ongeveer 1 g/mol.
* Zuurstof (O) heeft een molaire massa van ongeveer 16 g/mol.
* Dus de molaire watermassa (H₂o) is 2 (1 g/mol) + 16 g/mol =18 g/mol.
2. Bereken het aantal mol water:
* We hebben 18 gram water.
* Omdat 1 mol water 18 gram weegt, hebben we 18 gram / 18 g / mol =1 mol water.
3. Gebruik het nummer van Avogadro:
* Het nummer van Avogadro stelt dat er 6.022 x 10²³ moleculen in één mol van elke stof zijn.
* Daarom zijn er in 1 mol water 6,022 x 10²³ moleculen.
Daarom zijn er 6,022 x 10²³ watermoleculen in 18 gram water.
 Verbindingen in een Aziatische gefermenteerde vispasta kunnen een hoog cholesterolgehalte verlagen
Verbindingen in een Aziatische gefermenteerde vispasta kunnen een hoog cholesterolgehalte verlagen Wat produceert ATP NADH en CO2?
Wat produceert ATP NADH en CO2?  Onderzoekers ontwikkelen hoogwaardige keramische brandstofcel die werkt op butaangas
Onderzoekers ontwikkelen hoogwaardige keramische brandstofcel die werkt op butaangas De kubieke vorm van een mineraal kristal is hoogstwaarschijnlijk het resultaat dat kristal?
De kubieke vorm van een mineraal kristal is hoogstwaarschijnlijk het resultaat dat kristal?  Uit hoeveel atomen bestaat het element H2CO3?
Uit hoeveel atomen bestaat het element H2CO3?
Hoofdlijnen
- Wat vond Lamarck dat evolutie betrokken was waardoor zijn idee onjuist was?
- De ziekte is gemakkelijker te verspreiden in de samenleving?
- Welk type natuurfenonenom wordt uitgelegd in Ceres Proserpina?
- Waarom zebravissen (bijna) altijd strepen hebben
- Wat in de wetenschappelijke methode?
- Wat kan er met een organisme gebeuren als het orgaansysteem niet goed functioneert?
- Zeesterren zien:de ontbrekende schakel in de oogevolutie?
- Volgens het principe dat bekend staat als welke genen die onafhankelijk gescheiden zijn, beïnvloeden elke erfenis niet?
- Wat zijn de vier basiseenheden afgeleid van voedsel?
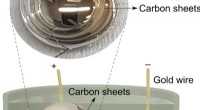
- Vloeibare metalen breken organische brandstoffen af tot ultradunne grafietplaten
- Origami en kirigami gebruiken om herconfigureerbare maar structurele materialen te inspireren

- Wetenschappers ontwikkelen luchtkwaliteitssensor die het leven van baby's en astmapatiënten kan redden

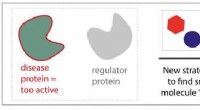
- Hoe moleculaire lijmen te vinden om ziekten effectief aan te pakken?
- Een prebiotische route naar DNA
 Op grafeen gebaseerde sensor detecteert schadelijke luchtvervuiling in huis
Op grafeen gebaseerde sensor detecteert schadelijke luchtvervuiling in huis Rook van Amerikaanse branden bereikt Europa, satellietgegevens laten zien
Rook van Amerikaanse branden bereikt Europa, satellietgegevens laten zien Onderzoekers modelleren plasmonische convectie op macroschaal om de beweging van vloeistof en deeltjes te beheersen
Onderzoekers modelleren plasmonische convectie op macroschaal om de beweging van vloeistof en deeltjes te beheersen Het kleinste element ter wereld?
Het kleinste element ter wereld?  Nieuwe vaardigheden leiden tot hogere salarissen, blijkt uit onderzoek
Nieuwe vaardigheden leiden tot hogere salarissen, blijkt uit onderzoek Wat is de fysieke hoeveelheid en SI -eenheid van ingeblikte drankjes?
Wat is de fysieke hoeveelheid en SI -eenheid van ingeblikte drankjes?  Kun je planeten van sterren vertellen met het blote oog?
Kun je planeten van sterren vertellen met het blote oog?  Waarom mensen lange tijd machines zullen verslaan bij het herkennen van spraak
Waarom mensen lange tijd machines zullen verslaan bij het herkennen van spraak
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

