
Wetenschap
Zoek de term elektronegativiteit op en leg uit hoe kan helpen bij het bepalen van het type chemische bindingen die in een verbinding bestaan?
Elektronegativiteit:de sleutel tot bindtype
Elektronegativiteit is een maat voor het vermogen van een atoom om elektronen aan te trekken in een chemische binding. Het is een waardevol hulpmiddel om de aard van chemische bindingen te begrijpen, met name bij het voorspellen of een binding ionisch zal zijn , covalent , of ergens tussenin ( polaire covalent ).
Hier is hoe elektronegativiteit helpt:
1. Elektronegativiteitswaarden vergelijken:
* Groot verschil in elektronegativiteit: Wanneer twee atomen een groot verschil hebben in elektronegativiteit (meestal groter dan 1,7), zal het meer elektronegatief atoom de gedeelde elektronen sterk aantrekken, waardoor ze in wezen "stelen" van het minder elektronegatieve atoom. Dit resulteert in de vorming van een ionische binding , waarbij het ene atoom positief wordt geladen (kation) en het andere negatief wordt geladen (anion).
* klein verschil in elektronegativiteit: Wanneer het verschil in elektronegativiteit klein is (typisch minder dan 0,5), worden de elektronen meer gelijk gedeeld tussen de twee atomen. Dit resulteert in een covalente binding , waar de atomen bij elkaar worden gehouden door het delen van elektronen.
* Intermediair verschil in elektronegativiteit: Als het verschil in elektronegativiteit tussen 0,5 en 1,7 daalt, wordt de binding beschouwd als polaire covalent . In dit geval worden de elektronen ongelijk gedeeld, wat leidt tot een gedeeltelijke positieve lading op het minder elektronegatieve atoom en een gedeeltelijke negatieve lading op het meer elektronegatieve atoom.
Voorbeeld:
* NaCl: Natrium (NA) heeft een elektronegativiteit van 0,93, terwijl chloor (CL) een elektronegativiteit van 3,16 heeft. Het grote verschil (2.23) geeft een ionische binding aan . Chloor "steelt" het elektron van natrium, vormt een natriumkation (Na+) en een chloride-anion (Cl-).
* H2: Waterstof (H) heeft een elektronegativiteit van 2.2. Omdat beide waterstofatomen dezelfde elektronegativiteit hebben, is de binding covalent waarbij de elektronen gelijk worden gedeeld.
* h2o: Zuurstof (O) heeft een elektronegativiteit van 3,44, terwijl waterstof een elektronegativiteit van 2,2 heeft. Het verschil (1.24) geeft een polaire covalente binding aan , met het zuurstofatoom met een gedeeltelijke negatieve lading en de waterstofatomen met gedeeltelijke positieve ladingen.
Samenvattend:
Elektronegativiteit is een fundamenteel concept waarmee we het type chemische binding tussen atomen kunnen voorspellen op basis van hun vermogen om elektronen aan te trekken. Dit begrip helpt ons de eigenschappen van verbindingen te interpreteren en hun gedrag te voorspellen in chemische reacties.
 Wie ontdekte de subatomaire deeltjes en in welke volgorde?
Wie ontdekte de subatomaire deeltjes en in welke volgorde?  Een stuk ijzer met een gewicht van 85,65 g werd in lucht verbrand de massa De geproduceerde oxide 118,37 Molair gebruiken om gebruikte mollen om te zetten?
Een stuk ijzer met een gewicht van 85,65 g werd in lucht verbrand de massa De geproduceerde oxide 118,37 Molair gebruiken om gebruikte mollen om te zetten?  Wat is het verschil tussen alchemisten en wetenschappers?
Wat is het verschil tussen alchemisten en wetenschappers?  Welke compound is CUF2?
Welke compound is CUF2?  Wat is CO2-afvang en waarom komt dit steeds ter sprake op COP28?
Wat is CO2-afvang en waarom komt dit steeds ter sprake op COP28?
 Geef twee voorbeelden van lange dagplanten en kort neutraal?
Geef twee voorbeelden van lange dagplanten en kort neutraal?  CO2-sensoren in twee stedelijke gebieden registreerden een grote daling van de uitstoot tijdens de COVID-19-pandemie
CO2-sensoren in twee stedelijke gebieden registreerden een grote daling van de uitstoot tijdens de COVID-19-pandemie Fracking laat een zware voetafdruk achter in Patagonië in Argentinië
Fracking laat een zware voetafdruk achter in Patagonië in Argentinië Meer dan een kopie:OCO-3 op het ruimtestation
Meer dan een kopie:OCO-3 op het ruimtestation Kunnen dikhoorns, een kogeltrein en een enorm zonnepark naast elkaar bestaan in de Mojave-woestijn?
Kunnen dikhoorns, een kogeltrein en een enorm zonnepark naast elkaar bestaan in de Mojave-woestijn?
Hoofdlijnen
- Wat doen rode bloedcellen in de hersenen?
- Wat in een koelkast voorkomt dat bacteriën en schimmels op het eten komen?
- Onderzoekers ontdekken hoe gelei-zeedieren moderne robotica kunnen vormen
- We hebben allemaal contacten nodig – hoe organellen elkaar omhelzen in cellen
- Onderzoek wijst achteruitgang van arctische kustvogels aan
- Wat is thermonoloog?
- Wat zijn de stadia van biologische verwering?
- Welk cijfer zou het meest nuttig zijn voor het tonen van complexe processen zoals celdeling?
- Hoe helpt Mimicry de kans op het overleven van een organismen te vergroten?
- Wetenschappers ontdekken dat de chemie van zware elementen kan veranderen bij hoge druk

- Rood, wit maar zelden blauw - de wetenschap van vuurwerkkleuren, uitgelegd

- Problemen met bellen vermijden:onderzoek naar de relatie tussen bellen en elektrochemie

- Wetenschappers produceren hoogwaardig gips volledig uit afval

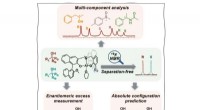
- Fluor maakt scheidingsvrije chirale chromatografische analyse mogelijk
 Cyberdreigingen voor geconnecteerde auto's
Cyberdreigingen voor geconnecteerde auto's Welke van de grote gassen bevat warmte?
Welke van de grote gassen bevat warmte?  Graslandgebieden moeten verstandig worden gekozen
Graslandgebieden moeten verstandig worden gekozen Hoe kan een botsing tussen continentale platen resulteren in de vorming van metamorf rots?
Hoe kan een botsing tussen continentale platen resulteren in de vorming van metamorf rots?  Kans op grote aardbeving in San Andreas vergroot door Ridgecrest temblors, studie suggereert:
Kans op grote aardbeving in San Andreas vergroot door Ridgecrest temblors, studie suggereert: Trinidad Java en Kyushu zijn voorbeelden van wat voor soort fysiek kenmerk?
Trinidad Java en Kyushu zijn voorbeelden van wat voor soort fysiek kenmerk?  Hoe lang leeft een ster die 1,2 keer de massa zon heeft?
Hoe lang leeft een ster die 1,2 keer de massa zon heeft?  Het glazen plafond:drie redenen waarom het nog steeds bestaat en de economie schaadt
Het glazen plafond:drie redenen waarom het nog steeds bestaat en de economie schaadt
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

