
Wetenschap
Wat is het pH -bereik van het resulterende product van koolstofdioxide en limwater?
Dit is waarom:
* Limewater is eenvoudig: Limwater is een oplossing van calciumhydroxide, een sterke basis, waardoor het zeer alkalisch is met een pH groter dan 7.
* CO2 is zuur: Koolstofdioxide lost op in water om koolzuur te vormen (H2CO3), een zwak zuur.
* neutralisatie: Wanneer CO2 door limwater wordt geborreld, reageert het zure koolzuur met het basiscalciumhydroxide, waardoor de oplossing wordt geneutraliseerd.
* Vorming van calciumcarbonaat: Deze neutralisatiereactie produceert calciumcarbonaat (CACO3), die onoplosbaar is in water en een wit neerslag vormt.
* pH -verandering: De pH van de oplossing neemt af naarmate het carbonzuur het calciumhydroxide neutraliseert, waardoor het dichter bij een neutrale pH van 7 komt.
Daarom heeft het resulterende product (calciumcarbonaat) zelf geen pH -bereik. De pH van de oplossing neemt echter af naarmate de reactie verloopt, en beweegt van het zeer alkalische bereik van limwater naar een meer neutrale pH.
Belangrijke opmerking: Het exacte pH -bereik van de resulterende oplossing zou afhangen van de initiële concentratie van limewater en de hoeveelheid CO2 toegevoegd.
Hoofdlijnen
- Hoeveel cellen zijn er in het menselijk lichaam?
- Wat wordt er weergegeven als geen enkele kopie van een allel de expressie maskeert?
- Waarom gooit mijn kat overal kattenbakvulling? Vier tips van kattenexperts
- Dierenartsen voeren de eerste bekende hersenoperatie uit om hydrocephalus bij pelsrobben te behandelen
- Aanpassen aan fluctuerende temperaturen
- Wat is het cellichaam van zenuwcel?
- Wat zijn twee cel -aanhangsels die de cellen helpen bewegen?
- Wat zijn enkele voorbeelden van aaseters in een zoetwaterbioom?
- Het is een slecht jaar voor Californische zalm. Hier ziet u hoe het de economie en het milieu schaadt
- Gelijktijdige meting van biofysische eigenschappen en positie van afzonderlijke cellen in een microdevice

- Eencellige test kan precies onthullen hoe medicijnen kankercellen doden

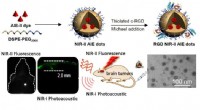
- Nieuwe methode helpt orthotope beeldvorming van hersentumoren duidelijker en sneller te maken
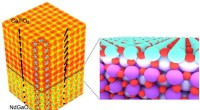
- Een 3D-beeldvormingstechniek ontgrendelt eigenschappen van perovskietkristallen
- Mangaan drukt zijn stempel op de synthese van geneesmiddelen

 Hoe een temperatuurstijging van 1,5 graden Celsius aanzienlijke veranderingen bij kustsoorten kan veroorzaken
Hoe een temperatuurstijging van 1,5 graden Celsius aanzienlijke veranderingen bij kustsoorten kan veroorzaken  Waarom is het belangrijk voor wetenschappers om informatie hun eigen onderzoek te delen?
Waarom is het belangrijk voor wetenschappers om informatie hun eigen onderzoek te delen?  Als de baan van een komeet 5000 keer afstand is tussen Pluto en zon in welke regio deze in?
Als de baan van een komeet 5000 keer afstand is tussen Pluto en zon in welke regio deze in?  De ergste vormen van dakloosheid komen minder vaak voor in Schotland dan in Engeland
De ergste vormen van dakloosheid komen minder vaak voor in Schotland dan in Engeland Wat betekenen de a en b in een enkele vervangingsreactie?
Wat betekenen de a en b in een enkele vervangingsreactie?  Nieuwe techniek zet antilichamen efficiënt om in sterk afgestemde nanobodies
Nieuwe techniek zet antilichamen efficiënt om in sterk afgestemde nanobodies Revolutionaire camera legt NASA's krachtigste raket in verbluffend detail vast
Revolutionaire camera legt NASA's krachtigste raket in verbluffend detail vast  Is het ooit dag op de maan?
Is het ooit dag op de maan?
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com


