
Wetenschap
Waarom wordt kopersulfaatoplossing helder en ontwikkelt magnesium een coating?
De reactie:
Wanneer u een stuk magnesiummetaal in een kopersulfaatoplossing plaatst, treedt de volgende reactie op:
mg (s) + cuso₄ (aq) → mgso₄ (aq) + cu (s)
Verklaring:
1. magnesium is reactiever dan koper: Magnesium is hoger op de reactiviteitsreeks dan koper. Dit betekent dat het waarschijnlijker is om elektronen te verliezen en positieve ionen te vormen.
2. Verplaatsing: Magnesiumatomen (mg) verplaatsen de koperionen (Cu²⁺) van de kopersulfaatoplossing (CUSO₄).
3. Vorming van magnesiumsulfaat: De magnesiumionen (mg²⁺) combineren vervolgens met sulfaationen (dus₄²⁻) om magnesiumsulfaat (mgso₄) te vormen, die oplost in het water.
4. Koperafzetting: De verplaatste koperionen (Cu²⁺) krijgen elektronen en worden vaste koperatomen (Cu), die het magnesiummetaal bedekken.
Observaties:
* Blauwe kopersulfaatoplossing wordt duidelijk: De blauwe kleur van de kopersulfaatoplossing komt van de koperionen (Cu²⁺). Naarmate de koperionen worden verplaatst en vast koper vormen, verliest de oplossing zijn blauwe kleur en wordt het duidelijk.
* magnesium ontwikkelt een coating: De vaste koperatomen afgezet op het magnesiummetaal vormen een roodbruine coating.
Samenvattend: De reactie wordt aangedreven door de grotere reactiviteit van magnesium, wat leidt tot de verplaatsing van koperionen uit de oplossing en de vorming van een koperen coating op het magnesium.
 Twee nauw verwante vijgensoorten vertonen tekenen van hybridisatie aan de klimaatmarges
Twee nauw verwante vijgensoorten vertonen tekenen van hybridisatie aan de klimaatmarges  Recordsmelt:Groenland verloor 586 miljard ton ijs in 2019
Recordsmelt:Groenland verloor 586 miljard ton ijs in 2019 Wetenschappers onthullen mineralogische en geochemische kenmerken van met koolwaterstof gebleekte rotsen in moddervulkanen
Wetenschappers onthullen mineralogische en geochemische kenmerken van met koolwaterstof gebleekte rotsen in moddervulkanen Ondanks de winst in Brazilië blijft de vernietiging van bossen hardnekkig hoog:rapport
Ondanks de winst in Brazilië blijft de vernietiging van bossen hardnekkig hoog:rapport  Vermindering van houtverbranding door plattelandsmensen in China leidt tot minder vervuiling door fijnstof
Vermindering van houtverbranding door plattelandsmensen in China leidt tot minder vervuiling door fijnstof
Hoofdlijnen
- Waarom wordt de cultuurbouillon voortdurend gemengd?
- Argentijnse wetenschappers maken zich zorgen na golf van walvissterfte
- Wat is dominant en recessief allel?
- Wat is de definitie van plasticiteit van de hersenen?
- Samengestelde gezichten van DNA helpen bij het oplossen van koude gevallen
- Heeft een wortelhaarcel cytoplasma?
- Wat hebben de drie soorten natuurlijke selectie gemeen?
- Zijn alle levende wezens van cellen een component de celtheorie?
- Wanneer een cel zich splitst in twee genetisch identieke dochtercellen?
- Biocompatibele fotonische kristallen breiden toepassingen uit van optica tot medicijnen
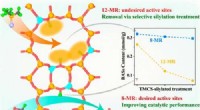
- Nieuwe strategie om de verspreiding van zuurplaatsen in zeolieten te beheersen
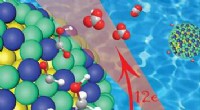
- Nieuwe core-shell-katalysator voor ethanolbrandstofcellen
- Hoe gestresste tumorcellen aan celdood ontsnappen:nieuw mechanisme ontdekt
- Team ontwikkelt afscheider die gasovergang voor waterelektrolyse vermindert

 Hoe thalassostatische terrassen zijn gevormd?
Hoe thalassostatische terrassen zijn gevormd?  Opwarming van de oceaan om verhoogde CO2-gedreven productiviteit teniet te doen
Opwarming van de oceaan om verhoogde CO2-gedreven productiviteit teniet te doen Welke planeet was de eerste die door ruimtevaartuigen werd bezocht?
Welke planeet was de eerste die door ruimtevaartuigen werd bezocht?  Nieuw wiskundig model geeft weer hoe de geest het sequentiële geheugen verwerkt en kan helpen bij het begrijpen van psychiatrische stoornissen
Nieuw wiskundig model geeft weer hoe de geest het sequentiële geheugen verwerkt en kan helpen bij het begrijpen van psychiatrische stoornissen  Spintronica:elektronica verbeteren met fijnere spincontrole
Spintronica:elektronica verbeteren met fijnere spincontrole OKE, computer:laten we tekstgenererende kunstmatige intelligentie in de klas brengen
OKE, computer:laten we tekstgenererende kunstmatige intelligentie in de klas brengen Verborgen geheimen van Orions-wolken
Verborgen geheimen van Orions-wolken Onderzoeksvraag:krimpt de maan?
Onderzoeksvraag:krimpt de maan?
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

