
Wetenschap
Bij een constante temperatuur neemt de druk uit die wordt uitgeoefend door één mol gas af als de beschikbare volume wordt verhoogd?
Dit is waarom:
* Druk en volume zijn omgekeerd evenredig: De wet van Boyle stelt dat bij een constante temperatuur de druk van een gas omgekeerd evenredig is met zijn volume. Dit betekent dat als u het volume van een gas verhoogt, de druk evenredig zal afnemen en vice versa.
* moleculaire botsingen: Druk in een gas wordt veroorzaakt door de botsingen van gasmoleculen met de wanden van hun container. Wanneer u het volume verhoogt, hebben de moleculen meer ruimte om te bewegen. Dit betekent dat ze minder vaak met de wanden botsen, wat resulteert in een lagere druk.
Wiskundige weergave:
De wet van Boyle wordt wiskundig uitgedrukt als:
P₁v₁ =p₂v₂
waar:
* P₁ is de initiële druk
* V₁ is het eerste volume
* P₂ is de uiteindelijke druk
* V₂ is het laatste deel
Voorbeeld:
Als u het volume van een gas verdubbelt terwijl u de temperatuur constant houdt, neemt de druk met de helft af.
 Houtindustrie Effect op waterverontreiniging
Houtindustrie Effect op waterverontreiniging  Nieuwe regels verduidelijken hoe objecten licht absorberen en uitstralen
Nieuwe regels verduidelijken hoe objecten licht absorberen en uitstralen  Jonge boeren in Californië vinden nieuwe manieren om vee te fokken en het land te verbeteren
Jonge boeren in Californië vinden nieuwe manieren om vee te fokken en het land te verbeteren Onderschatting van geïrrigeerde gewassen leidt tot watertekorten
Onderschatting van geïrrigeerde gewassen leidt tot watertekorten Hij zag een kernbomtest op de Marshalleilanden van dichtbij. Het achtervolgt hem sinds 1952
Hij zag een kernbomtest op de Marshalleilanden van dichtbij. Het achtervolgt hem sinds 1952
Hoofdlijnen
- Welke rol speelt RNA in genexpressie?
- Grootte van witrotschimmels verklaard door de breedte van de betrokken genfamilies
- Hoe ontrouw neven en nichten helpt:mannen delen mogelijk meer genen met de kinderen van zussen dan met vreemdgaande echtgenotes
- Praat je tegen mij? Wetenschappers proberen het mysterie van 'dierlijke gesprekken' te ontrafelen
- Hoe reageert het immuunsysteem op veranderde zwaartekracht?
- Ozonvervuiling bedreigt de gezondheid van planten en maakt het voor bestuivers moeilijker om bloemen te vinden
- Grenzen van het uithoudingsvermogen als marathonsterren geen tijd meer hebben
- Waarom zijn decomposers belangrijk in een ecosysteem?
- Waar komt al het goud vandaan?
- Verbindingen in een Aziatische gefermenteerde vispasta kunnen een hoog cholesterolgehalte verlagen

- Rioolschat:ingenieurs onthullen hoe ze processen kunnen optimaliseren voor het omzetten van zwavel in afvalwater in waardevolle materialen

- Detectie van fermentatieprocessen in elektriciteitopwekkende bacteriën

- Wetenschappers ontwikkelen een nieuw apparaat om geavanceerde kristallijne materialen te screenen

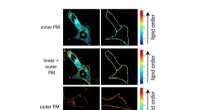
- Lipidenasymmetrie speelt een sleutelrol bij het activeren van immuuncellen
 Hoe versterkers per seconde in elektronen om te zetten
Hoe versterkers per seconde in elektronen om te zetten Membraanloze protocellen kunnen aanwijzingen geven voor de vorming van het vroege leven
Membraanloze protocellen kunnen aanwijzingen geven voor de vorming van het vroege leven Hoe beschrijft u de beweging van de beweging en koolstofdioxide tussen levende wezens in het milieu?
Hoe beschrijft u de beweging van de beweging en koolstofdioxide tussen levende wezens in het milieu?  Eigenschappen van isopropylalcohol
Eigenschappen van isopropylalcohol Welke planeet heeft het helderste ringsysteem?
Welke planeet heeft het helderste ringsysteem?  Supernova-explosies worden ondersteund door neutrino's van neutronensterren, een nieuwe waarneming suggereert:
Supernova-explosies worden ondersteund door neutrino's van neutronensterren, een nieuwe waarneming suggereert: Waarom is het aardklimaat niet te warm noch koud?
Waarom is het aardklimaat niet te warm noch koud?  Is water een colloïde of suspensie -oplossing?
Is water een colloïde of suspensie -oplossing?
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

