
Wetenschap
Hoeveel gram H2 zijn er nodig om 5,51 mol Cuo in de reactie te verminderen?
Hier is hoe dit probleem op te lossen:
1. Evenwichtige chemische vergelijking:
De reactie tussen koperoxide (CuO) en waterstofgas (H₂) is:
Cuo + H₂ → Cu + H₂o
2. Mol -verhouding:
Uit de evenwichtige vergelijking zien we dat 1 mol H₂ reageert met 1 mol Cuo.
3. Berekening:
Omdat we 5,51 mol Cuo hebben, hebben we een gelijke hoeveelheid H₂ nodig om volledig te reageren.
Daarom hebben we 5.51 mol H₂ nodig .
4. Converteer mollen naar gram:
Om mol H₂ om te zetten in gram, gebruiken we de molaire massa van H₂ (2.016 g/mol).
Massa van H₂ =(5,51 mol H₂) * (2.016 g/mol) = 11,1 g H₂
Antwoord: Je hebt 11,1 gram h₂ nodig om 5,51 mol Cuo te verminderen.
 NASA vangt de aanlanding van India van tropische depressie Phethai
NASA vangt de aanlanding van India van tropische depressie Phethai Wat veroorzaakt de meeste verwering op het aardoppervlak?
Wat veroorzaakt de meeste verwering op het aardoppervlak?  Satelliethorloges overblijfselen van tropische storm Harvey bij Honduras
Satelliethorloges overblijfselen van tropische storm Harvey bij Honduras GPM-satelliet ziet lichte regen in tropische depressie 33Ws oostkant
GPM-satelliet ziet lichte regen in tropische depressie 33Ws oostkant IPCC, 's werelds hoogste autoriteit op het gebied van klimaatwetenschap
IPCC, 's werelds hoogste autoriteit op het gebied van klimaatwetenschap
Hoofdlijnen
- In een plant verklaart de drukstroomhypothese de beweging van suiker van naar de?
- In het Ecuadoraanse Amazonegebied vormen vlinders een graadmeter voor de klimaatverandering
- De geesten van HeLa:hoe verkeerde identificatie van cellijnen de wetenschappelijke literatuur besmet
- Gebruik van DNA Extraction
- Golgi -lichamen gebruiken wat moleculen uit de cel transporteren?
- Wat zijn drie gebieden van hypothese -evolutie?
- Reproductie waar is er maar één ouder?
- Wat zijn de principes en doelen van ergonomie?
- Wat is osmose en welke osmotische druk?
- Verbetering van de waarneming van eiwitbinding

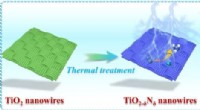
- Surface defect engineering van nanodraadarrays naar efficiënte stikstofreductie voor ammoniaksynthese
- Groene chemici vinden een manier om cashewnootdoppen om te zetten in zonnebrandcrème
- Lab-on-a-disc-technologie belooft te versnellen, DNA-analyse ter plaatse vereenvoudigen

- Eenvoudige watertest kan verlammende botziekte voorkomen

 Hoe is de wetenschap begonnen?
Hoe is de wetenschap begonnen?  Onderzoekers camoufleren een optische chip waardoor deze onzichtbaar wordt
Onderzoekers camoufleren een optische chip waardoor deze onzichtbaar wordt Hoe klimaatverhalen mensen helpen om door complexiteit te navigeren en oplossingen te vinden
Hoe klimaatverhalen mensen helpen om door complexiteit te navigeren en oplossingen te vinden Ideale methode voor het snel testen van ziekten
Ideale methode voor het snel testen van ziekten De kracht van licht voor internet van onderwaterdingen
De kracht van licht voor internet van onderwaterdingen Welke kracht is verantwoordelijk voor de revolutie van planeten rond de zon?
Welke kracht is verantwoordelijk voor de revolutie van planeten rond de zon?  Wetenschappers vechten om het regenwoud van DR Congo te beschermen terwijl de bedreigingen toenemen
Wetenschappers vechten om het regenwoud van DR Congo te beschermen terwijl de bedreigingen toenemen Komt natuurlijk? Wandelende wandelende takken gebruiken om natuurlijke selectie en de voorspelbaarheid van evolutie te bestuderen
Komt natuurlijk? Wandelende wandelende takken gebruiken om natuurlijke selectie en de voorspelbaarheid van evolutie te bestuderen
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

