
Wetenschap
Wat is de evenwichtige ionische vergelijking voor wanneer ammoniumfosfaat reageert met natriumhydroxide?
1. Schrijf de onevenwichtige moleculaire vergelijking:
(NH₄) ₃po₄ (aq) + NaOH (aq) → Na₃po₄ (aq) + nH₃ (g) + h₂o (l)
2. Identificeer de toeschouwersionen:
* toeschouwersionen zijn ionen die aan beide zijden van de vergelijking verschijnen en niet deelnemen aan de werkelijke reactie.
* In dit geval zijn de toeschouwersionen na⁺ en po₄³⁻.
3. Schrijf de volledige ionische vergelijking:
3nh₄⁺ (aq) + po₄³⁻ (aq) + na⁺ (aq) + oh⁻ (aq) → 3na⁺ (aq) + po₄³⁻ (aq) + nh₃ (g) + h₂o (l)
4. Annuleer de toeschouwersionen:
3NH₄⁺ (aq) + oh⁻ (aq) → nH₃ (g) + h₂o (l)
5. De evenwichtige ionische vergelijking:
NH₄⁺ (aq) + oh⁻ (aq) → nH₃ (g) + h₂o (l)
Verklaring:
* De reactie produceert ammoniakgas (NH₃) en water (H₂o) als producten.
* Het ammoniumion (NH₄⁺) werkt als een zuur en doneert een proton (H⁺) aan het hydroxide -ion (OH⁻), en vormt ammoniak en water.
* Dit is een neutralisatiereactie tussen een zwakke basis (ammoniak) en een sterke basis (natriumhydroxide).
 Wat is het smeltpunt van FECL3?
Wat is het smeltpunt van FECL3?  Kopercoating op 3D-geprinte plastic filters voorgesteld als een pandemische strijder
Kopercoating op 3D-geprinte plastic filters voorgesteld als een pandemische strijder Wat zijn de fluorverbindingen?
Wat zijn de fluorverbindingen?  Hoe de grootte van een atoom te karakteriseren
Hoe de grootte van een atoom te karakteriseren  Wat is de algemene naam voor een vaste stof die wordt geproduceerd in chemische reactie die de oplossing bewolkt maakt?
Wat is de algemene naam voor een vaste stof die wordt geproduceerd in chemische reactie die de oplossing bewolkt maakt?
 Terug uit de dood:hoe je een verloren soort weer tot leven kunt wekken
Terug uit de dood:hoe je een verloren soort weer tot leven kunt wekken  Klimaatverandering begrijpen als een maatschappelijk probleem
Klimaatverandering begrijpen als een maatschappelijk probleem Waarom de aarde nu een koerscorrectie nodig heeft
Waarom de aarde nu een koerscorrectie nodig heeft Weinig realistische scenario's over om de opwarming van de aarde te beperken tot 1,5°C
Weinig realistische scenario's over om de opwarming van de aarde te beperken tot 1,5°C Groen van woede:vrouwelijke leiders in klimaatverandering worden geconfronteerd met online aanvallen
Groen van woede:vrouwelijke leiders in klimaatverandering worden geconfronteerd met online aanvallen
Hoofdlijnen
- Wat is speciaal aan de structuur van groeihormoon?
- Wetenschappers verdelen dieren in twee groepen op basis van het feit of een dier een ruggengraat heeft. Waar onwaar.?
- Wat is DNA -polymerase -proeflezen?
- Hoe ureum de toegangspoort tot het leven kan zijn geweest
- Wat is de naam van organel die betrokken is bij zuurstof die proces vereist door welke energie -macromoleculen ATP heeft opgeslagen?
- Hoe worden eiwitten van elkaar onderscheiden?
- Waar wordt glucose opgeslagen nadat de plant tijdens fotosynthese heeft gemaakt?
- De wetenschap boekt vooruitgang op het gebied van veroudering. Maar willen we eeuwig leven?
- Wat betekent cultusss in de wetenschap?
- Nieuw apparaat kan warmte-energie omzetten in een levensvatbare brandstofbron
- Onderzoekers valideren klinische haalbaarheid voor op CRISPR gebaseerde COVID-19-tests op het zorgpunt
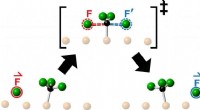
- Poreus kristal leidt reactie om koolstofdioxide te transformeren

- Groene chemie en biobrandstof:het mechanisme van een sleutelfoto-enzym gedecodeerd

- Ontdekking van domino-chemie opent nieuwe grenzen in reactiedynamiek
 Wat is innerlijk membraaneiwit en uiterlijk hoe kun je van E. coli krijgen hoe je het eiwit kunt scheiden?
Wat is innerlijk membraaneiwit en uiterlijk hoe kun je van E. coli krijgen hoe je het eiwit kunt scheiden?  Heb je een zoetekauw? Geef je lever de schuld
Heb je een zoetekauw? Geef je lever de schuld  Welk stuk land ging de mens naar Amerika?
Welk stuk land ging de mens naar Amerika?  Wat gebeurt er als zilvernitraat aan bariumchloride wordt toegevoegd?
Wat gebeurt er als zilvernitraat aan bariumchloride wordt toegevoegd?  Een nieuwe manier om aardbevingen waar te nemen, kan systemen voor vroegtijdige waarschuwing helpen verbeteren
Een nieuwe manier om aardbevingen waar te nemen, kan systemen voor vroegtijdige waarschuwing helpen verbeteren Welk type variabelen zijn er in het experiment?
Welk type variabelen zijn er in het experiment?  Waarom komen sommige mineralen alleen voor in metamorfe rotsen?
Waarom komen sommige mineralen alleen voor in metamorfe rotsen?  Wat zijn cellen met dezelfde functie georganiseerd?
Wat zijn cellen met dezelfde functie georganiseerd?
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

