
Wetenschap
Is C3H6BR2 polair of niet -polair?
* Moleculaire geometrie: Het centrale koolstofatoom in 1,2-dibromopropaan wordt gebonden aan twee broomatomen, één waterstofatoom en een CH2-groep. Dit resulteert in een tetrahedral Geometrie rond de centrale koolstof.
* Elektronegativiteitsverschil: Bromine (BR) is meer elektronegatief dan koolstof (C) en waterstof (H). Dit betekent dat de broomatomen de elektronendichtheid naar zichzelf trekken, waardoor gedeeltelijke negatieve ladingen (δ-) worden gecreëerd op de broomatomen en gedeeltelijke positieve ladingen (δ+) op de koolstof- en waterstofatomen.
* Dipoolmoment: Het ongelijke delen van elektronen creëert een dipoolmoment binnen elke C-BR-binding. Omdat het molecuul niet symmetrisch is, annuleren deze dipoolmomenten elkaar niet. In plaats daarvan combineren ze om een netto dipoolmoment te creëren voor het hele molecuul.
Daarom maakt de aanwezigheid van een netto dipoolmoment 1,2-dibromopropaan een polair molecuul.
 Wat zijn de drie componenten die fossiele brandstoffen moesten vormen?
Wat zijn de drie componenten die fossiele brandstoffen moesten vormen?  Eenfasige covalente organische raamwerkmembranen maken CO2-selectieve scheiding mogelijk
Eenfasige covalente organische raamwerkmembranen maken CO2-selectieve scheiding mogelijk Legeronderzoeker gebruikt wiskunde om nieuwe scheikunde te ontdekken
Legeronderzoeker gebruikt wiskunde om nieuwe scheikunde te ontdekken Wordt H2O2 alleen opgesplitst door organische katalysator?
Wordt H2O2 alleen opgesplitst door organische katalysator?  Wat doet de bimetallische strip in een thermostaat?
Wat doet de bimetallische strip in een thermostaat?
Hoofdlijnen
- Wat is de medische term die een wetenschapper betekent die aids bestudeert?
- Zijn eiwitten in een cel levend?
- Wordt gist sneller of langzamer groeit met meer suiker?
- Hoeveel van onze hersenen gebruiken we? De mythe ontkrachten
- Wanneer ouderplanten worden gekruist, hoe verwijzen wetenschappers naar de eerste generatie nakomelingen?
- Waar zijn de chromosomen gelegen in een normale cel?
- Genetische analyses laten zien hoe symbiotische bacteriën in de termietendarm in de loop van de evolutie zijn veranderd
- Nieuw inzicht in waarom de ziekte van Pierce zo dodelijk is voor wijnstokken
- Hoe beantwoordt een wetenschapper de wetenschappelijke vraag?
- Een soort mos kan medisch effectiever blijken te zijn dan hennep

- Activering van prodrug met behulp van in eiwit omhulde goudkatalysator
- Wetenschappers vereenvoudigen het proces om polymeren te maken met door licht geactiveerde nanodeeltjes

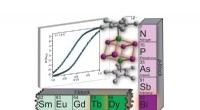
- Onderzoekers maken een magneet gemaakt van één molecuul
- Supercomputers sturen onderzoek naar ionentransport aan
 Heeft vorm invloed op de luchtweerstand op een object?
Heeft vorm invloed op de luchtweerstand op een object?  Hebben alle niet -metalen een volledig volle valentie -schaal van elektronen?
Hebben alle niet -metalen een volledig volle valentie -schaal van elektronen?  Young Inventors Fair Ideas
Young Inventors Fair Ideas Welke beroemde vulkaan is omgeven door een meer?
Welke beroemde vulkaan is omgeven door een meer?  Quiz:Hoeveel weet u over Stephen Hawking?
Quiz:Hoeveel weet u over Stephen Hawking?  Hoe veilig zijn vier- en zescijferige pincodes voor mobiele telefoons?
Hoe veilig zijn vier- en zescijferige pincodes voor mobiele telefoons? Een vliegtuig gebruiken om vluchtige organische stoffen te meten uit dagbouwinstallaties in oliezanden
Een vliegtuig gebruiken om vluchtige organische stoffen te meten uit dagbouwinstallaties in oliezanden Video:Kip Thorne vertelt over de jaren voorafgaand aan LIGO's eerste detectie van zwaartekrachtsgolven
Video:Kip Thorne vertelt over de jaren voorafgaand aan LIGO's eerste detectie van zwaartekrachtsgolven
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

