
Wetenschap
Waarom groep 4 metalen vormen ionen?
* Elektronenconfiguratie: Groep 4 metalen hebben 4 valentie -elektronen (elektronen in de buitenste schaal). Dit betekent dat ze relatief dicht bij het hebben van een volledige buitenste schaal, wat een stabiele configuratie is.
* ionisatie -energie: Deze metalen hebben relatief lage ionisatie -energieën, wat betekent dat het niet veel energie nodig heeft om elektronen uit hun buitenschalen te verwijderen.
* elektropositiviteit: Groep 4 metalen zijn elektropositief, wat betekent dat ze de neiging hebben elektronen te verliezen en kationen te worden (positief geladen ionen).
Hoe ze ionen vormen:
1. Verlies van elektronen: Om een stabiele elektronenconfiguratie te bereiken, verliezen groep 4 metalen meestal hun 4 valentie -elektronen. Dit laat hen een +4 lading en vormt ionen zoals Ti⁴⁺, Zr⁴⁺ en HF⁴⁺.
2. Vorming van ionische bindingen: Deze positief geladen ionen vormen vervolgens gemakkelijk ionische bindingen met negatief geladen niet -metalen, zoals zuurstof (o²⁻) of chloor (CL⁻), waardoor verbindingen zoals titaniumdioxide (Tio₂) of zirkoniumchloride (ZRCL₄) ontstaan.
belangrijke opmerkingen:
* variabele oxidatietoestanden: Hoewel de +4 oxidatietoestand het meest voorkomt, kunnen groep 4 metalen ook andere oxidatietoestanden, zoals +2 en +3, in bepaalde verbindingen vertonen.
* Reactiviteit: De reactiviteit van groep 4 metalen neemt de groep af. Titanium is relatief reactief, terwijl zirkonium en hafnium minder reactief zijn.
* Toepassingen: Groep 4 metalen en hun verbindingen hebben verschillende toepassingen vanwege hun unieke eigenschappen, waaronder hoge smeltpunten, sterkte en weerstand tegen corrosie. Voorbeelden zijn gebruik in ruimtevaart, medische implantaten en pigmenten.
Samenvattend, de neiging om een stabiele elektronenconfiguratie, lage ionisatie -energie en elektropositieve natuuraandrijfgroep 4 metalen te bereiken om elektronen te verliezen en ionen te vormen. Dit leidt tot de vorming van ionische bindingen en een breed scala aan verbindingen met waardevolle toepassingen.
 Innovatieve biogebaseerde luchtfilter kan luchtfiltratie transformeren, mogelijk allergenen in de lucht binnenshuis verminderen
Innovatieve biogebaseerde luchtfilter kan luchtfiltratie transformeren, mogelijk allergenen in de lucht binnenshuis verminderen Doorbraak in het mengen van metalen - nauwkeurige controle van multimetallische clustervorming van één nanometer bereikt
Doorbraak in het mengen van metalen - nauwkeurige controle van multimetallische clustervorming van één nanometer bereikt Gebruik van Thermoplastics
Gebruik van Thermoplastics Wijn met een dubbele shot vitamine C?
Wijn met een dubbele shot vitamine C?  In welk type massabeweging kunnen bodems zich een vloeistof gedragen en stromen?
In welk type massabeweging kunnen bodems zich een vloeistof gedragen en stromen?
Hoofdlijnen
- Een groene kleur wordt veroorzaakt door de aanwezigheid van welk organel?
- Vampiervleermuizen bestuderen om de volgende pandemie te voorspellen
- Wat is een niet-voorbeeld van de wetenschappelijke theorie?
- Genetische analyses onthullen nieuwe virussen aan de horizon
- Wat doet de plant met voedsel dat zijn cellen niet kunnen gebruiken?
- Cellen in een celkweek hebben allemaal hetzelfde genetische materiaal omdat het A. vectoren zijn B. Plasmiden C. Hybriden D. klonen?
- Wat zijn de twee vormen van wetenschappelijke methode?
- Hoe ongewenste componenten uit de celkern te verwijderen
- Hittetolerante broccoli voor de toekomst
- Een nieuw regime voor het analyseren van eigenschappen van topologische materialen

- Chemische ingenieurs bevorderen de productie van olefinen door middel van computationele modellering

- Ontwikkeling van een 3D-deeltjesmodel voor afzonderlijke deeltjes in batterij-elektroden
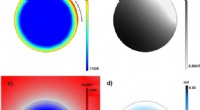
- Upconversie-fluorescentie in metalen organische raamwerken

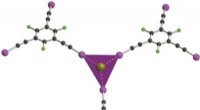
- Coördinatiechemie van anionen door halogeenbindingsinteracties
 Waarom is de contellatie Leo zichtbaar in het oosten op een avond van januari, maar in West juli -avond?
Waarom is de contellatie Leo zichtbaar in het oosten op een avond van januari, maar in West juli -avond?  Welke term definieert een proces dat de gemiddelde eigenschappen van een organisme vermeldt?
Welke term definieert een proces dat de gemiddelde eigenschappen van een organisme vermeldt?  Hoeveel 200 AMP -panelen kunt u op 250 kVA -transformator aftappen?
Hoeveel 200 AMP -panelen kunt u op 250 kVA -transformator aftappen?  Onderzoekers ontwikkelen een unieke methode om poedercomposieten te maken
Onderzoekers ontwikkelen een unieke methode om poedercomposieten te maken Wat is de wetenschappelijke naam van chloor?
Wat is de wetenschappelijke naam van chloor?  Hoe gemengde getallen en oneigenlijke breuken terug te brengen naar de laagste voorwaarden
Hoe gemengde getallen en oneigenlijke breuken terug te brengen naar de laagste voorwaarden  Waarom heeft napthalene een hoog kookpunt?
Waarom heeft napthalene een hoog kookpunt?  Hoe lang duurde het voordat Apollo ruimte kreeg en weer terug?
Hoe lang duurde het voordat Apollo ruimte kreeg en weer terug?
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

