
Wetenschap
Waarom is methaan exotherme?
Dit is waarom:
* exotherme reacties Laat energie vrij in de omgeving, meestal als warmte.
* verbranding is een chemische reactie waarbij een stof snel reageert met een oxidatiemiddel, typisch zuurstof, om warmte en licht te produceren.
De verbranding van methaan (CH4) met zuurstof (O2) produceert koolstofdioxide (CO2) en water (H2O) samen met warmte en licht:
CH4 + 2O2 → CO2 + 2H2O + warmte + licht
Hier is de uitsplitsing waarom deze reactie exotherme is:
* Bond breken: Het verbreken van de bindingen in methaan en zuurstof vereist energie.
* Bondvorming: Het vormen van de bindingen in koolstofdioxide en water geeft energie vrij.
* Energiebalans: De energie die vrijkomt tijdens de vorming van bindingen in de producten is groter dan de energie die nodig is om de bindingen in de reactanten te verbreken. Dit verschil in energie wordt vrijgegeven als warmte, waardoor de reactie exotherme wordt.
Daarom is methaan zelf niet exotherme. De exotherme reactie is de verbranding van methaan, waarbij de energie die wordt vrijgegeven door nieuwe bindingen te vormen groter dan de energie die nodig is om bestaande bindingen te verbreken.
 Waarom is de oppervlaktespanning van water hoger dan die van methaan?
Waarom is de oppervlaktespanning van water hoger dan die van methaan?  Welke van deze elementen is geen diatome stikstofbroom zuurstofcalcium?
Welke van deze elementen is geen diatome stikstofbroom zuurstofcalcium?  Organische verbindingen zijn veelbelovend als goedkopere alternatieven voor metaalfotokatalysatoren
Organische verbindingen zijn veelbelovend als goedkopere alternatieven voor metaalfotokatalysatoren  Reageert ijzer met geconcentreerd salpeterzuur?
Reageert ijzer met geconcentreerd salpeterzuur?  MRI-techniek detecteert de eigenschappen van verpakt vlees
MRI-techniek detecteert de eigenschappen van verpakt vlees
 Klimaatvragen:Wie is het meest kwetsbaar voor klimaatverandering?
Klimaatvragen:Wie is het meest kwetsbaar voor klimaatverandering?  4e graad Science Fair Projectideeën
4e graad Science Fair Projectideeën  Door de opwarming van de aarde zullen ecosystemen meer methaan produceren dan eerst werd voorspeld
Door de opwarming van de aarde zullen ecosystemen meer methaan produceren dan eerst werd voorspeld Rook van Canadese branden drijft de Verenigde Staten binnen
Rook van Canadese branden drijft de Verenigde Staten binnen Onderzoek is gericht op het voorkomen van sterfgevallen als gevolg van emissies van gipsgebonden mest
Onderzoek is gericht op het voorkomen van sterfgevallen als gevolg van emissies van gipsgebonden mest
Hoofdlijnen
- Doodt oceaanafval walvissen?
- Chimpansees zijn geen huisdieren, ongeacht wat sociale media je vertellen
- Twee artikelen beschrijven hoe een membraaneiwit zowel lipiden als ionen kan verplaatsen
- Welk stadium zijn chromosomen gedupliceerd?
- Absorberen gistcellen neutrale rode kleurstof?
- Waardoor stinkt de durian-vrucht? Kankerwetenschappers kraken het durian-genoom
- Beschrijf de structuur van nucleotiden en leg uit hoe ze belangrijk zijn voor levende dingen?
- Wat zijn de stappen van de stikstofcyclus?
- Hoe heeft Florida niet gereageerd op een epizoötische koraalziekte en wat volgt?
- Gemodificeerde biomaterialen zelf-assembleren op temperatuursignalen

- Het benutten van verloren atomen kan helpen bij het maken van nieuwe, nooit eerder vertoonde oxiden
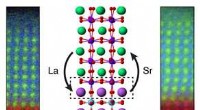
- Extreem sterke en toch ongelooflijk ductiele meercomponentenlegeringen ontwikkeld

- Zonneverdamper biedt een frisse route naar zoet water

- Lichtgevende gels voor een groot aantal toepassingen, van namaak tot bio-sensing
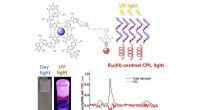
 Hoe ontstaan zandsteenschalie en kalksteen?
Hoe ontstaan zandsteenschalie en kalksteen?  Heeft racisme Jackie Robinson vermoord?
Heeft racisme Jackie Robinson vermoord? De effecten van maansverduisteringen
De effecten van maansverduisteringen  Ontbossing Amazone en aantal branden tonen zomer 2019 geen normaal jaar
Ontbossing Amazone en aantal branden tonen zomer 2019 geen normaal jaar Wat was Kepers -theorie?
Wat was Kepers -theorie?  Wat is de relatie van Moons met zee?
Wat is de relatie van Moons met zee?  James Webb Telescope:een wetenschapper legt uit wat de eerste verbazingwekkende afbeeldingen laten zien en hoe het de astronomie zal veranderen
James Webb Telescope:een wetenschapper legt uit wat de eerste verbazingwekkende afbeeldingen laten zien en hoe het de astronomie zal veranderen Voordelige, herbruikbare Mn-katalysatoren zorgen voor een efficiënte alkylering van ketonen met alcoholen
Voordelige, herbruikbare Mn-katalysatoren zorgen voor een efficiënte alkylering van ketonen met alcoholen
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

