
Wetenschap
Combineren atomen in slechts één-op-één verhoudingen om verbindingen te vormen?
Dit is waarom:
* chemische formules: Verbindingen worden weergegeven door chemische formules, die de typen en aantallen aanwezige atomen laten zien. Deze formules kunnen verschillende verhoudingen hebben, niet alleen 1:1.
* Voorbeelden:
* water (h₂o): Twee waterstofatomen combineren met één zuurstofatoom.
* koolstofdioxide (co₂): Eén koolstofatoom combineert met twee zuurstofatomen.
* Natriumchloride (NaCl): Eén natriumatoom combineert met één chlooratoom (dit is een verhouding van 1:1, maar het is niet de enige mogelijkheid).
* valentie -elektronen: Het aantal elektronen dat een atoom kan delen of doneren om obligaties te vormen, bepaalt de verhoudingen waarin atomen combineren. Sommige elementen kunnen meerdere bindingen vormen, wat leidt tot verschillende verhoudingen in verbindingen.
Samenvattend: Atomen combineren in verschillende verhoudingen om verbindingen te vormen, afhankelijk van de specifieke betrokken elementen en hun elektronenconfiguraties.
 Wat zijn twee redenen waarom interdisciplinaire wetenschap belangrijk is?
Wat zijn twee redenen waarom interdisciplinaire wetenschap belangrijk is?  Wetenschappers bestuderen vissen om te leren hoe ze de gevolgen van klimaatverandering kunnen aanpassen
Wetenschappers bestuderen vissen om te leren hoe ze de gevolgen van klimaatverandering kunnen aanpassen  Wat is een goede zin voor behoud?
Wat is een goede zin voor behoud?  Nieuw VN-rapport onthult onthutsende menselijke klimaatvoetafdruk op water en ijs
Nieuw VN-rapport onthult onthutsende menselijke klimaatvoetafdruk op water en ijs Frequente hete zomers in Europa/West-Azië en Noordoost-Azië na het midden van de jaren negentig
Frequente hete zomers in Europa/West-Azië en Noordoost-Azië na het midden van de jaren negentig
Hoofdlijnen
- Wat is de basiseenheid van een structuur en functie in een organisme dat wordt genoemd?
- Rudolph, waarom is je neus zo helder? Wetenschappers van Johns Hopkins hebben een idee
- Wat is de symbiotische relatie tussen pathogeen en een mens?
- Enzymcomplexen die eiwitten afbreken heten?
- Welke twee weefsels kunnen niet zo gemakkelijk regenereren?
- Wat zijn vier verschillende organismen?
- Hoe samenwerking de concurrentie bij apen kan overtroeven
- Facebook-aandelen 'liken'? Deskundigen wegen in op de beursgang
- Onderzoekers ontdekken hoe cellen bewegen terwijl ze adhesie vermijden
- Een complete set van energieniveauposities van alle primaire metaalhalogenideperovskieten
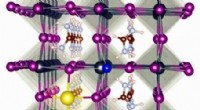
- Nieuwe zuurbestendige membranen voor afvalwaterzuivering ontwikkeld
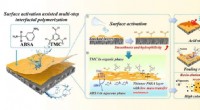
- Nieuwe oppervlaktebehandeling kan de koelingsefficiëntie verbeteren

- Duurzaam waterzuiveringssysteem geïnspireerd door de natuur

- Belangrijke mijlpaal op weg naar overgangsmetaalkatalyse met aluminium
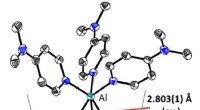
 Maak een lijst van de lagen van de aarde door hun chemische samenstelling en fysische eigenschappen?
Maak een lijst van de lagen van de aarde door hun chemische samenstelling en fysische eigenschappen?  Wat is gerelateerd aan de maan?
Wat is gerelateerd aan de maan?  Welke organel in een plant laat glucose uit zonlicht komen?
Welke organel in een plant laat glucose uit zonlicht komen?  Slimme kruispunten kunnen de congestie van autonome auto's verminderen
Slimme kruispunten kunnen de congestie van autonome auto's verminderen Wetenschappers ontwikkelen nieuwe, snellere methode om donkere materie op te sporen
Wetenschappers ontwikkelen nieuwe, snellere methode om donkere materie op te sporen Gebruikt een landgebaseerd telefoongebruik elektriciteit?
Gebruikt een landgebaseerd telefoongebruik elektriciteit?  Voormalige Twitter-medewerker verkocht privégegevens van mensen aan de Saoedi-Arabische overheid
Voormalige Twitter-medewerker verkocht privégegevens van mensen aan de Saoedi-Arabische overheid Model toont Welshe taal die niet met uitsterven wordt bedreigd, maar te reo Māori is op weg naar buiten
Model toont Welshe taal die niet met uitsterven wordt bedreigd, maar te reo Māori is op weg naar buiten
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

