
Wetenschap
Wat is het doel van elektrolyse?
* Niet-spontane reacties: Dit zijn chemische reacties die niet van nature op zichzelf voorkomen. Ze vereisen een externe energie -input om door te gaan.
* elektriciteit als energie -input: Elektrolyse biedt die energie -input door de stroom van elektrische stroom.
* Chemische reacties aansturen: De elektrische stroom zorgt ervoor dat ionen in een oplossing (of gesmolten zout) migreren naar elektroden met tegengestelde ladingen. Deze migratie leidt tot chemische veranderingen bij de elektroden, wat resulteert in de gewenste reactie.
in eenvoudiger termen: Elektrolyse is als het gebruik van elektriciteit om een chemische reactie te laten plaatsvinden die normaal niet op zichzelf zou optreden.
Hier zijn enkele belangrijke toepassingen van elektrolyse:
* Productie van elementen: Elektrolyse wordt gebruikt om zuivere metalen (zoals aluminium, natrium en chloor) uit hun verbindingen te extraheren.
* Elektropatisering: Een metalen object bedekken met een dunne laag van een ander metaal om het uiterlijk, de corrosieweerstand of de elektrische geleidbaarheid te verbeteren.
* watersplitsing: Elektrolyse van water produceert waterstof en zuurstofgas. Dit is een veelbelovende methode voor het produceren van schone, hernieuwbare energie.
* Synthese van chemicaliën: Elektrolyse speelt een rol bij de productie van verschillende chemicaliën, zoals natriumhydroxide en chloorgas.
Laat het me weten als je specifieke voorbeelden van elektrolyse in meer detail wilt verkennen!
 Wetenschappers modelleren nauwkeurig de werking van aerosolen op wolken
Wetenschappers modelleren nauwkeurig de werking van aerosolen op wolken Inzicht in de bodemgesteldheid voor stormen helpt wetenschappers om zware regenval in moessongebieden te voorspellen
Inzicht in de bodemgesteldheid voor stormen helpt wetenschappers om zware regenval in moessongebieden te voorspellen Afvalwater heeft de richting van de seismische spanning in het zuiden van Kansas niet significant veranderd
Afvalwater heeft de richting van de seismische spanning in het zuiden van Kansas niet significant veranderd Het mysterie van hoe kevers die in watervoerende lagen leven, is opgelost
Het mysterie van hoe kevers die in watervoerende lagen leven, is opgelost  Welke vogels nestelen op de grond?
Welke vogels nestelen op de grond?
Hoofdlijnen
- Wat is een verklaring op basis van wetenschappelijke kennis?
- Hoe denken wetenschappers?
- Wat betekent het dat een cel multiponent is?
- Vorm geven aan de manier waarop de vervormbaarheid van rode bloedcellen wordt beoordeeld:onderzoekers ontwikkelen een nieuwe aanpak
- Hoe ziet een kern eruit?
- Langzaam bevroren mensen? Recent onderzoek ondersteunt de mogelijkheid van cryopreservatie
- Wat zijn de orgaansystemen in het menselijk lichaam en hoe homeostase te relateren?
- Wat wordt bedoeld met fitness in de darwinistische evolutie?
- Uit onderzoek blijkt hoe microplastics in de luchtwegen van mensen blijven hangen
- Nauwkeurige deuteratie met zwaar water
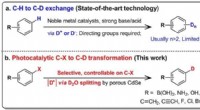
- Energieteam ontwikkelt processen om biogebaseerde vliegtuigbrandstof op te voeren

- Nieuwe synthesestrategie versnelt identificatie van eenvoudigere versies van een natuurlijk product

- Nieuw type glas geïnspireerd door de natuur is beter bestand tegen schokken
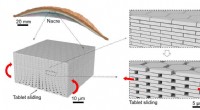
- Baanbrekend materiaal maakt weg naar waterstofgebruik voor brandstofcellen onder heet, droge omstandigheden
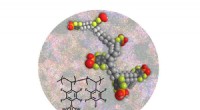
 Hoe het aantal combinaties te berekenen
Hoe het aantal combinaties te berekenen Wat kunt u zeggen over de relatieve grootten van roosterergie -ammoniumchloride en de warmtehydratatie ervan?
Wat kunt u zeggen over de relatieve grootten van roosterergie -ammoniumchloride en de warmtehydratatie ervan?  Twee elektronen in helium worden slechts één schaal geplaatst terwijl drie lithium twee schelpen bezetten?
Twee elektronen in helium worden slechts één schaal geplaatst terwijl drie lithium twee schelpen bezetten?  Wat is een zure basisindicator?
Wat is een zure basisindicator?  Nieuwe inzichten in fermentatie-enzymen zullen de ecologische voetafdruk van de chemische industrie verkleinen
Nieuwe inzichten in fermentatie-enzymen zullen de ecologische voetafdruk van de chemische industrie verkleinen Waarom voeg je chloor toe aan kraanwater?
Waarom voeg je chloor toe aan kraanwater?  Wat is het pad van licht door het oog?
Wat is het pad van licht door het oog?  Welke mineralen en gesteenten worden in Turkije gevonden?
Welke mineralen en gesteenten worden in Turkije gevonden?
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

