
Wetenschap
Wat zijn inert en labiele liganden?
inert en labiele liganden:een snelle uitsplitsing
inerte liganden Vorm sterke bindingen met het centrale metaalion, waardoor ze resistent zijn tegen substitutiereacties. Ze blijven zelfs gehecht in aanwezigheid van andere potentiële liganden.
labiele liganden Vorm zwakke bindingen met het centrale metaalion, waardoor ze gemakkelijk worden vervangen door andere liganden. Ze zijn vatbaar voor substitutiereacties, zelfs in aanwezigheid van zwakke nucleofielen.
Hier is een meer gedetailleerde uitleg:
Inerte liganden:
* Sterke M-L-bindingen: Deze liganden vormen sterke coördinaatbindingen met het metaalion, vaak vanwege:
* Hoge ladingsdichtheid op het ligand: Zeer geladen liganden zoals CN- en NH3 vormen sterkere bindingen.
* Klein formaat van het ligand: Kleinere liganden kunnen dichter bij het metaalion komen, wat leidt tot sterkere attracties.
* aanwezigheid van π-backbonding: Dit omvat donatie van elektronen van de metaal D-orbitalen aan lege orbitalen op het ligand, waardoor de binding verder wordt versterkt.
* Slow Ligand Exchange: De sterke band maakt het voor andere liganden moeilijk om ze te verplaatsen. Dit vertaalt zich in langzame snelheden van substitutiereacties.
Labiele liganden:
* Zwakke M-L-bindingen: Deze liganden vormen relatief zwakke coördinaatbindingen met het metaalion, vaak vanwege:
* Lage ladingsdichtheid op het ligand: Zwak geladen liganden zoals H2O en Cl- vormen zwakkere bindingen.
* Groot formaat van het ligand: Grotere liganden zijn verder van het metaalion, wat leidt tot zwakkere interacties.
* afwezigheid van π-backbonding: Geen extra stabilisatie van elektronendonatie tot ligand orbitalen.
* snelle liganduitwisseling: De zwakke binding maakt het gemakkelijk voor andere liganden om ze te verplaatsen. Dit vertaalt zich in snelle tarieven van substitutiereacties.
belangrijke punten:
* Inertheid en labiliteit zijn kinetische termen: Ze beschrijven de * snelheid * van ligandsubstitutie, niet de thermodynamische stabiliteit van het complex. Een thermodynamisch stabiel complex kan nog steeds labiel zijn als de liganduitwisseling snel is.
* factoren die inertie/labiliteit beïnvloeden:
* Aard van het metaalion: Overgangsmetalen met hogere ladingen en kleinere ionische stralen hebben de neiging om meer inerte complexen te vormen.
* Aard van de liganden: Liganden met een hoge ladingsdichtheid en klein formaat zijn eerder inert.
* oplosmiddel: Polaire oplosmiddelen kunnen de overgangstoestand stabiliseren, waardoor substitutiereacties sneller worden.
Voorbeelden:
* inert: Complexen met CN-, NH3 en CO-liganden zijn meestal inert.
* labile: Complexen met H2O, Cl- en br-liganden zijn meestal labiel.
Toepassingen:
Inzicht in de concepten van inerte en labiele liganden is cruciaal op verschillende gebieden:
* Coördinatiechemie: Het voorspellen van de stabiliteit en reactiviteit van coördinatiecomplexen.
* katalyse: Katalysatoren ontwerpen met specifieke ligandomgevingen voor het bevorderen van bepaalde reacties.
* Biochemistry: Het gedrag van metaalionen in biologische systemen uitleggen.
Laat het me weten als je nog vragen hebt over deze concepten.
 Mudskipper-robot laat zien hoe gewervelde dieren evolueerden om op het land te lopen
Mudskipper-robot laat zien hoe gewervelde dieren evolueerden om op het land te lopen  Valse verhalen beweren dat NASA bekende lithium te hebben verspreid
Valse verhalen beweren dat NASA bekende lithium te hebben verspreid Hoe leren we jongeren over klimaatverandering? We kunnen beginnen met deze strip
Hoe leren we jongeren over klimaatverandering? We kunnen beginnen met deze strip Waarom regenval in sommige gebieden hoog is en waarom laag?
Waarom regenval in sommige gebieden hoog is en waarom laag?  Hoe bewegen aardwormen?
Hoe bewegen aardwormen?
Hoofdlijnen
- Wat is escologie?
- Wat kan tot speciatie leiden?
- Licht werpend op hoe bacteriën met elkaar omgaan
- Hoeveel cellagen heeft rondworm?
- Zal klimaatverandering het risico op aflatoxine in Amerikaanse maïs vergroten?
- In welk type cel is kern gevonden?
- Zet de volgende structuren in volgorde van klein naar groot:chromosoom, genoom, nucleotidebasis, codon, gen, celkern?
- Wat zijn vier belangrijkste takken van de mariene wetenschap?
- Het echte verschil tussen plantaardige en dierlijke cellen
- Klittenbandachtige voedselsensor detecteert bederf en besmetting

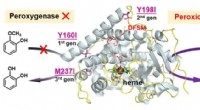
- P450-peroxygenase omzetten in peroxidase via mechanismegestuurde eiwittechnologie
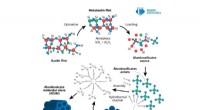
- 'S Werelds eerste biobricks gekweekt uit menselijke urine

- Stof gevonden in fossiele brandstoffen kan veranderen in pure diamant

- Chemicus creëert katalysator om anti-muggenstoffen te produceren
 Hoe schrijf je 0,34 in standaardvorm?
Hoe schrijf je 0,34 in standaardvorm?  Inkjetprinters kunnen goedkope microgolfgeleiders voor optische computers produceren
Inkjetprinters kunnen goedkope microgolfgeleiders voor optische computers produceren Wat moet je weten om een versnelling te berekenen?
Wat moet je weten om een versnelling te berekenen?  Hoe lang duurt het om van de maan van de aarde te gaan met mensen erop?
Hoe lang duurt het om van de maan van de aarde te gaan met mensen erop?  Wat is een afgeleide UNTIT?
Wat is een afgeleide UNTIT?  Hoe zwaar of dicht een rots is hoe hij het noemde?
Hoe zwaar of dicht een rots is hoe hij het noemde?  3D Hoe een bril werkt
3D Hoe een bril werkt  Wie is de grootste wetenschapper aller tijden?
Wie is de grootste wetenschapper aller tijden?
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

