
Wetenschap
Hoe de pH te meten met behulp van waterstofelektrode?
Inzicht in de waterstofelektrode
* principe: De waterstofelektrode is een referentie -elektrode die een standaardpotentiaal vaststelt op basis van het evenwicht tussen waterstofionen (H+) en waterstofgas (H2). Het is de basis van de pH -schaal.
* Setup: Een platina -elektrode wordt ondergedompeld in een oplossing die waterstofionen bevat. Waterstofgas wordt over het elektrode -oppervlak geborreld.
* Nernst -vergelijking: Het potentieel van de elektrode is direct gerelateerd aan de concentratie van waterstofionen (en dus de pH) via de Nernst -vergelijking:
E =e ° + (rt/nf) * ln (ah +)
Waar:
* E =elektrodepotentiaal
* E ° =standaard elektrodepotentiaal (0,000 V bij 25 ° C)
* R =ideale gasconstante
* T =absolute temperatuur
* n =aantal overgedragen elektronen (1 in dit geval)
* F =constant van Faraday
* ah+ =activiteit van waterstofionen (ongeveer gelijk aan concentratie in verdunde oplossingen)
procedure
1. Bereid de waterstofelektrode:
* Zorg ervoor dat de platina -elektrode schoon is en vrij van verontreinigingen.
* Verzadig de oplossing met waterstofgas (gebruik een bubbler).
* Houd een constante druk van waterstofgas.
2. Bereid de referentie -elektrode voor:
* Gebruik een standaard referentie -elektrode (bijv. Een verzadigde calomel -elektrode (SCE) of zilver/zilverchloride -elektrode (AG/AGCL)).
3. Sluit de elektroden aan:
* Sluit de waterstofelektrode en de referentie-elektrode aan op een hoge-impedantie voltmeter of pH-meter.
4. Dompel de elektroden onder:
* Dompel de elektroden onder in de oplossing waarvan u de pH wilt meten.
5. Meet het potentiaalverschil:
* De voltmeter geeft het potentiaalverschil weer tussen de waterstofelektrode en de referentie -elektrode.
6. Bereken de pH:
* Gebruik de Nernst -vergelijking om de pH te berekenen uit het gemeten potentiaalverschil. Als alternatief zijn veel pH -meters gekalibreerd om de pH -waarde direct weer te geven.
belangrijke overwegingen
* Temperatuur: De Nernst-vergelijking is temperatuurafhankelijk. Zorg ervoor dat de temperatuur bekend is en verantwoord in de berekening.
* Oplossingscondities: De pH -meting kan worden beïnvloed door factoren zoals ionsterkte, opgeloste gassen en de aanwezigheid van redox -actieve soorten.
* Elektrode -stabiliteit: Waterstofelektroden kunnen gevoelig zijn voor vergiftiging door bepaalde stoffen. Handhaaf de juiste reinigings- en hanteringsprocedures.
Alternatieven voor waterstofelektroden
Hoewel waterstofelektroden fundamenteel zijn, zijn ze niet altijd praktisch. Andere, handiger methoden zijn beschikbaar voor het meten van pH, zoals:
* Glazen elektroden: Dit zijn de meest voorkomende en veel gebruikte elektroden voor pH -meting. Ze zijn relatief goedkoop, gemakkelijk te gebruiken en draagbaar.
* Combinatie -elektroden: Deze elektroden integreren zowel de referentie -elektrode als de detectie -elektrode in een enkele eenheid, waardoor de opstelling wordt vereenvoudigd.
Laat het me weten als je een meer gedetailleerde uitleg van een van deze aspecten wilt, of als je andere vragen hebt over pH -metingen!
 De eerste succesvolle vervangers voor ivoren biljartballen werden gemaakt met celluloid versterkt met gemalen runderbot
De eerste succesvolle vervangers voor ivoren biljartballen werden gemaakt met celluloid versterkt met gemalen runderbot  Waarom jodium is bijna onoplosbaar in water, maar lost het gemakkelijk op een waterige oplossing van KI?
Waarom jodium is bijna onoplosbaar in water, maar lost het gemakkelijk op een waterige oplossing van KI?  Wat is een oplossing met pH groter dan 7?
Wat is een oplossing met pH groter dan 7?  Woordvergelijking voor de reactie van halogenen met natrium?
Woordvergelijking voor de reactie van halogenen met natrium?  Onthulling van wat de kristalgroei regelt
Onthulling van wat de kristalgroei regelt
 Hoe sloppenwijken veerkrachtiger kunnen worden tegen de klimaatverandering
Hoe sloppenwijken veerkrachtiger kunnen worden tegen de klimaatverandering  Indonesiërs verlaten hun huizen in de buurt van een uitbarstende vulkaan en de luchthaven sluit vanwege asgevaar
Indonesiërs verlaten hun huizen in de buurt van een uitbarstende vulkaan en de luchthaven sluit vanwege asgevaar  Vroeg smelten van winterse sneeuwval bevordert de Arctische lente
Vroeg smelten van winterse sneeuwval bevordert de Arctische lente Deze sociale wetenschap houdt zich bezig met hoe cultuur van generatie is doorgegeven, terwijl mensen veranderingen in milieutechnologie of verandering aanpassen. Zouden S?
Deze sociale wetenschap houdt zich bezig met hoe cultuur van generatie is doorgegeven, terwijl mensen veranderingen in milieutechnologie of verandering aanpassen. Zouden S?  Buitenonderwijs heeft enorme voordelen voor kinderen en leraren, dus waarom wordt het niet op meer scholen gebruikt?
Buitenonderwijs heeft enorme voordelen voor kinderen en leraren, dus waarom wordt het niet op meer scholen gebruikt?
Hoofdlijnen
- Studie ontdekt waarom guppies kleurrijk zijn
- Welk organisme vereist niet dat zonlicht leefte chemosynthetische bacterie bomen algen of fotosynthetische bacteriën?
- Opnieuw geïntroduceerde wolven doden vier jaarlingrunderen tijdens de laatste reeks veeaanvallen in Colorado
- Wat wordt specifiek met enzym bedoeld?
- Wat is de functie van substage in de microscoop?
- Onderzoeken hoe microbiomen onze gezondheid beïnvloeden
- Waarom zijn modellen nuttig in de wetenschap?
- Factoren die betrokken zijn bij celdifferentiatie
- Wat maken wetenschappers om hen een hypothese te helpen en gegevens te verzamelen?
- Nieuwe studies van oud beton zouden ons kunnen leren te doen zoals de Romeinen deden

- Dunne waterlagen zijn veelbelovend voor de energieopslag van de toekomst

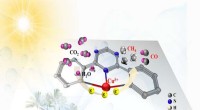
- Nieuwe katalysator verhoogt radicaal de omzettingssnelheid van koolstofdioxide in zonnebrandstoffen
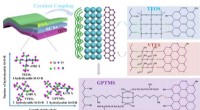
- Silaan reguleert de thermische geleidbaarheid van composieten op moleculair niveau
- Moleculen net zo gemakkelijk vastbinden als veters

 Voelt u zich zelfvoldaan over uw zonnedak? Niet zo snel
Voelt u zich zelfvoldaan over uw zonnedak? Niet zo snel  Wat is de zonne -ballon?
Wat is de zonne -ballon?  Gemakkelijk waarnemen van schadelijke stoffen die milieuvervuiling veroorzaken via de camera van een mobiele telefoon
Gemakkelijk waarnemen van schadelijke stoffen die milieuvervuiling veroorzaken via de camera van een mobiele telefoon  Hoe een motor met drie en drie fasen te voeden
Hoe een motor met drie en drie fasen te voeden Waarom is een boot op zee bewijs voor een ronde aarde?
Waarom is een boot op zee bewijs voor een ronde aarde?  Hoe luchtvaartpersoneel werkt
Hoe luchtvaartpersoneel werkt  Hoe heet een gemeenschap en zijn habitat?
Hoe heet een gemeenschap en zijn habitat?  Hoe wordt een covalente binding genoemd waarin elektronen gelijkelijk worden verdeeld?
Hoe wordt een covalente binding genoemd waarin elektronen gelijkelijk worden verdeeld?
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

