
Wetenschap
Wat bepaalt de verschillende isotopen van een atoom?
* Atomisch nummer: Dit definieert het element. Het wordt bepaald door het aantal protonen in de kern van een atoom. Alle koolstofatomen hebben bijvoorbeeld 6 protonen.
* Massienummer: Dit vertegenwoordigt het totale aantal protonen en neutronen in de kern van een atoom.
* isotopen: Atomen van hetzelfde element (hetzelfde atoomnummer) kunnen verschillende aantallen neutronen hebben. Deze variatie in neutronentelling leidt tot verschillende massagummers, waardoor isotopen worden gecreëerd.
Voorbeeld:
* carbon-12: Heeft 6 protonen en 6 neutronen (massaummer =12)
* carbon-14: Heeft 6 protonen en 8 neutronen (massaummer =14)
Beide zijn koolstofatomen omdat ze 6 protonen hebben, maar ze zijn isotopen vanwege het verschillende aantal neutronen.
Key Takeaways:
* Isotopen van hetzelfde element hebben dezelfde chemische eigenschappen omdat ze hetzelfde aantal elektronen hebben.
* Isotopen hebben verschillende fysieke eigenschappen zoals massa en dichtheid.
* Sommige isotopen zijn radioactief, wat betekent dat hun kernen na verloop van tijd straling uitzenden.
Ik hoop dat dit helpt! Laat het me weten als je nog vragen hebt.
 Speekseltest voor cannabis kan ooit helpen bij het identificeren van gehandicapte bestuurders
Speekseltest voor cannabis kan ooit helpen bij het identificeren van gehandicapte bestuurders Wat is coëfficiënten na plus Cl2 - NaCl?
Wat is coëfficiënten na plus Cl2 - NaCl?  Welk organischzuur dat in lage concentratie optreedt, is essentieel voor de mens maar zeer gevaarlijk wanneer mensen er hoog van worden blootgesteld?
Welk organischzuur dat in lage concentratie optreedt, is essentieel voor de mens maar zeer gevaarlijk wanneer mensen er hoog van worden blootgesteld?  Wat betekent het om te zeggen dat een atoom zich in een aangeslagen toestand bevindt?
Wat betekent het om te zeggen dat een atoom zich in een aangeslagen toestand bevindt?  Beschrijf kort de opstelling van moleculen in een vaste vloeistof en gas?
Beschrijf kort de opstelling van moleculen in een vaste vloeistof en gas?
Hoofdlijnen
- Wat is het classificatiesysteem dat in de biologie wordt gebruikt?
- Wetenschappers ontdekken hoe twee eiwitten helpen cellen gezond te houden
- Wat is de concentratie van zenuwweefsel en sensorische organen aan het voorste einde van een organisme?
- Wat bevat meestal eencellige organismen met kernen?
- Voors en tegens van Recombinant DNA Technology
- Wat worden cellen gevormd tijdens mitose?
- Uitbreiding tonijnquota stap achteruit voor instandhouding
- Hoe is ATP -synthase betrokken bij het maken van energie van de cel?
- Wat is eigenlijk haploïde?
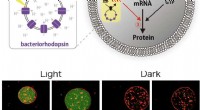
- Wetenschapper bouwt kunstmatige fotosynthetische cellen
- Natuurkundigen ontdekken een tri-aniondeeltje met kolossale stabiliteit

- Ontwikkeling van fluoralkylcarbonaten om de farmaceutische en chemische industrie schoner en veiliger te maken

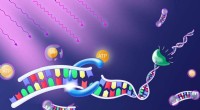
- Programmeren met de lichtschakelaar
- Selectieve synthese van meta-isomeren nu mogelijk
 Het retentie-effect van training
Het retentie-effect van training Kleine nanokubussen helpen wetenschappers links van rechts te onderscheiden
Kleine nanokubussen helpen wetenschappers links van rechts te onderscheiden Wat is de term voor het meten van land?
Wat is de term voor het meten van land?  Extreem snelle elektrochrome supercondensatoren
Extreem snelle elektrochrome supercondensatoren Amerikanen worden echt gek van apparaten die ze volgen en afluisteren
Amerikanen worden echt gek van apparaten die ze volgen en afluisteren Hebben we een categorie 6 nodig voor orkanen?
Hebben we een categorie 6 nodig voor orkanen?  Hoe bouw je een Black Hole voor een Science Fair Project
Hoe bouw je een Black Hole voor een Science Fair Project  Als radiosterrenstelsels botsen, superzware zwarte gaten vormen nauw verbonden paren
Als radiosterrenstelsels botsen, superzware zwarte gaten vormen nauw verbonden paren
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

