
Wetenschap
Wanneer een stof de substantie temperatuur smelt?
Dit is waarom:
* Faseverandering: Smelten is een faseverandering van vast tot vloeistof. Tijdens deze verandering wordt de energie toegevoegd aan de stof gebruikt om de bindingen tussen moleculen in de vaste toestand te verbreken, niet om hun kinetische energie te vergroten (wat zou leiden tot een temperatuurstijging).
* latente fusiewarmte: De energie die nodig is om de toestand van een substantie bij een constante temperatuur te veranderen, wordt de latent warmwarmte van fusie genoemd . Deze energie wordt geabsorbeerd door de stof terwijl deze smelt, waardoor de temperatuur constant blijft.
Zie het zo:stel je voor dat je warmte toevoegt aan een ijsblok. Het ijs zal de warmte absorberen en de temperatuur zal stijgen totdat het het smeltpunt bereikt (0 graden Celsius). Op dit punt verhoogt de warmte niet langer de temperatuur, maar wordt gebruikt om de bindingen tussen watermoleculen te verbreken, waardoor het ijs in vloeibaar water wordt veranderd. De temperatuur blijft op 0 graden Celsius totdat al het ijs is gesmolten.
Pas nadat alle stof is gesmolten, begint de toegevoegde warmte de temperatuur van de vloeistof te verhogen.
 Zou de volgende chemische vergelijking naoh aq plus hcl nacl s h2o l reactant van naoh kunnen zijn?
Zou de volgende chemische vergelijking naoh aq plus hcl nacl s h2o l reactant van naoh kunnen zijn?  Wordt een vaste stof veranderd van vloeistof naar gasfysische of chemische verandering?
Wordt een vaste stof veranderd van vloeistof naar gasfysische of chemische verandering?  Bij welke temperatuur en concentratie explodeert waterstof?
Bij welke temperatuur en concentratie explodeert waterstof?  E-waste transformeren in een sterk, beschermende coating voor metaal
E-waste transformeren in een sterk, beschermende coating voor metaal Welk metaal had de atomaire straal van 238 PM?
Welk metaal had de atomaire straal van 238 PM?
Hoofdlijnen
- Hoe een cel te splitsen in Two
- Herprogrammering van buiten naar binnen:antilichaamonderzoek suggereert een betere manier om stamcellen te maken
- Welk systeem bereidt voedsel voor op cellulair gebruik?
- Wat is de nadruk van het menselijke genoomproject?
- Wat verzamelt zuren om eiwitten te maken?
- Wat is de wetenschappelijke naam voor kunstmest?
- Hoe recyclen cellen de machinerie die hun beweeglijkheid aandrijft?
- Waarom worden cellen de basiseenheid van het leven genoemd?
- Hoe kunnen chemosynthetische organismen wetenschappers helpen te begrijpen hoe het leven op aarde is ontwikkeld?
- Nieuwe sensor test binnenkort mogelijk gelijktijdig op coronavirus en griep

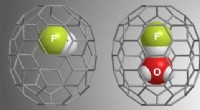
- Onderzoekers isoleren waterstoffluoride en water om zuuroplossing te begrijpen
- Onderzoek onthulde de allereerste kristalstructuur van de dopamine 2-receptor gebonden aan een antipsychoticum

- Een visuele database van menselijke plasmaverbindingen

- Machine learning biedt een nieuwe manier om chirale kristallen te ontwerpen

 Onderzoek naar motiverende verhalen van meth-gebruikers in Alabama is de eerste foto-etnografie in de criminologie
Onderzoek naar motiverende verhalen van meth-gebruikers in Alabama is de eerste foto-etnografie in de criminologie Onderzoekers creëren materialen met een unieke combinatie van stijfheid en thermische isolatie
Onderzoekers creëren materialen met een unieke combinatie van stijfheid en thermische isolatie  Digitale transformatie zal de sleutel zijn tot het voortbestaan van de theaterindustrie tijdens het coronavirus, uit onderzoek blijkt
Digitale transformatie zal de sleutel zijn tot het voortbestaan van de theaterindustrie tijdens het coronavirus, uit onderzoek blijkt Worden uw hersenen net zo moe als de rest van uw lichaam?
Worden uw hersenen net zo moe als de rest van uw lichaam?  Kiemvrije diermodellen onthullen de rol van darmbacteriën in de gezondheid
Kiemvrije diermodellen onthullen de rol van darmbacteriën in de gezondheid  Afleveringssystemen voor deeltjesvormige vaccins kunnen helpen beschermen tegen uitbraken van infectieziekten en bioterreurbedreigingen
Afleveringssystemen voor deeltjesvormige vaccins kunnen helpen beschermen tegen uitbraken van infectieziekten en bioterreurbedreigingen AI gebruiken om kraters op de maan te tellen en in kaart te brengen
AI gebruiken om kraters op de maan te tellen en in kaart te brengen Gedoemde komeet gespot nabij de zon tijdens de totale zonsverduistering van 8 april
Gedoemde komeet gespot nabij de zon tijdens de totale zonsverduistering van 8 april
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

