
Wetenschap
Wat is het volume van 0,323 mol gas zal bezetten op 265K en druk 0,900aTm?
U kunt dit oplossen met behulp van de ideale gaswet:
pv =nrt
Waar:
* p =Druk (in atmosferen)
* v =Volume (in liters)
* n =Aantal mol
* r =Ideale gasconstante (0,0821 L · atm/mol · k)
* t =Temperatuur (in kelvin)
1. Herschik de vergelijking om op te lossen voor V:
V =(nrt) / p
2. Sluit de gegeven waarden aan:
V =(0,323 mol * 0,0821 l · atm / mol · k * 265 k) / 0,900 atm
3. Bereken het volume:
V ≈ 8.02 l
Daarom zal het monster van 0,323 mol gas ongeveer 8,02 liter bezetten bij 265k en 0,900 atm.
 Nanomaterialen - korte polymeren, grote impact
Nanomaterialen - korte polymeren, grote impact Wat is het vriespunt van een oplossing gemaakt door het oplossen van 0,771 g bifenyl C12H10 in 25,0 g cyclohexaan?
Wat is het vriespunt van een oplossing gemaakt door het oplossen van 0,771 g bifenyl C12H10 in 25,0 g cyclohexaan?  Mistharp vergroot opvangcapaciteit voor schoon water
Mistharp vergroot opvangcapaciteit voor schoon water Onderzoekers stellen nieuwe technologie voor luchtvaartmaterialen voor om hun eigenschappen aan te passen
Onderzoekers stellen nieuwe technologie voor luchtvaartmaterialen voor om hun eigenschappen aan te passen Bacteriën groeien in agar
Bacteriën groeien in agar
Hoofdlijnen
- Research Paper Topics in Biochemistry
- Hoe mitochondriën een krachtige klap inzetten tegen levensbedreigende bacteriën
- Hoe is fosforylering belangrijk in een signaaltransductiecascade?
- Het zijn voornamelijk moeders die mitochondriën doorgeven - en een nieuwe theorie zegt dat dit te wijten is aan het eerste seksuele conflict
- Wetenschappers onthullen waarom buikwantsen zo goed door je darmen kunnen zwemmen
- Wat zijn drie locaties in het menselijk lichaam waar twee systemen contact maken?
- Hoe helpt de wetenschappelijke methode wetenschapper?
- Natuurbeschermers bevestigen opnieuw een aanval op grijze wolven in Jackson County in Colorado
- Hoe werken de verschillende soorten cellen om longen schoon te maken?
- Diepgaande leertechnieken leren het neurale model retrosynthese te spelen
- Onderzoek naar oxidatieve routes in nucleaire brandstof

- Genetische schakelaars bij kanker nader bekijken

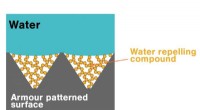
- Super waterafstotende materialen zijn nu duurzaam genoeg voor de echte wereld
- Video:De enige detox die je ooit nodig zult hebben

 Welke fasen doorloopt steenkool voordat het een diamant vormt?
Welke fasen doorloopt steenkool voordat het een diamant vormt?  Een metamorfe rots die niet gelaagd lijkt te zijn?
Een metamorfe rots die niet gelaagd lijkt te zijn?  GPD converteren naar MGD
GPD converteren naar MGD Fossiele voetafdrukken bewijzen dat mensen duizenden jaren eerder Amerika bevolkten dan we dachten
Fossiele voetafdrukken bewijzen dat mensen duizenden jaren eerder Amerika bevolkten dan we dachten Onderzoekers ontdekken een stukje Amerika in het noorden van Australië
Onderzoekers ontdekken een stukje Amerika in het noorden van Australië Waarom zijn kopernitraat en zwavel dezelfde kleur?
Waarom zijn kopernitraat en zwavel dezelfde kleur?  Bereken een mijl
Bereken een mijl Hoe krijgt de aarde al zijn energie?
Hoe krijgt de aarde al zijn energie?
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

