
Wetenschap
Gelijke mol H2O en NaCl zijn aanwezig in een oplossing, daarom is molariteit?
* Molariteit is mol opgeloste oplossing per liter oplossing.
* Water is zowel het oplosmiddel als een component van de oplossing. U moet het totale volume van de oplossing weten om de molariteit te berekenen.
Dit is wat je moet doen:
1. Bepaal het totale volume van de oplossing: Je moet het volume van het water plus het volume van de opgeloste NaCl kennen.
2. Bereken de molariteit:
* Verdeel het aantal mol NaCl (de opgeloste stof) door het totale volume van de oplossing in liters.
Voorbeeld:
Laten we zeggen dat je 1 mol H₂o en 1 mol NaCl hebt. Als het totale volume van de oplossing 2 liter is, dan:
* Molariteit van NaCl =1 mol / 2 liter =0,5 m
Belangrijke opmerking: Het volume van de oplossing zal waarschijnlijk verschillen van de som van de volumes van het water en NaCl. Dit komt omdat de oplossing van NaCl in water een volume -verandering kan veroorzaken.
 Onderzoekers geven eerste chemische kaart van kleurstoffen vrij uit historische kleurstofbibliotheek
Onderzoekers geven eerste chemische kaart van kleurstoffen vrij uit historische kleurstofbibliotheek Wat zijn de intermoleculaire krachten die betrokken zijn bij CH3OH?
Wat zijn de intermoleculaire krachten die betrokken zijn bij CH3OH?  Welke elementen zou u samen reageren om het samengestelde ijzersulfide te maken?
Welke elementen zou u samen reageren om het samengestelde ijzersulfide te maken?  Wat is celebrium traditionele metal?
Wat is celebrium traditionele metal?  Wat is het hoofdbestanddeel van lucht?
Wat is het hoofdbestanddeel van lucht?
 Gezondheid Zuidelijke Oceanen aangetast door eb en vloed van de rivier Murray
Gezondheid Zuidelijke Oceanen aangetast door eb en vloed van de rivier Murray Waarom krijgt de oostkust van Australië zoveel regen? Een atmosferische wetenschapper legt het uit
Waarom krijgt de oostkust van Australië zoveel regen? Een atmosferische wetenschapper legt het uit  Shell getroffen door Nederlandse klimaatrechtszaak
Shell getroffen door Nederlandse klimaatrechtszaak Post-tropische cycloon Prapiroons-resten bewegen over het noorden van Japan
Post-tropische cycloon Prapiroons-resten bewegen over het noorden van Japan VS bereikt record voor kostbare weerrampen:$ 306 miljard (update 2)
VS bereikt record voor kostbare weerrampen:$ 306 miljard (update 2)
Hoofdlijnen
- Wat zijn endorfines?
- Gezocht:vrijwillige schutters om kudde bizons in Grand Canyon uit te dunnen (update)
- Waar en waarom mensen schaatsen maakten van dierlijke botten
- Slagen, grote oceaanreservaten moeten zowel het zeeleven als de mensen ten goede komen
- Wat zijn drie nucleotiden op overdracht RNA die complementair zijn aan het RNA van de boodschapper?
- Wat is het exosysteem?
- Wat zijn de zes fasen van wetenschappelijk onderzoek?
- Schimmelparing:volgend wapen tegen maïsaflatoxine?
- Welk deel van de afscheidingen van de celpakketten?
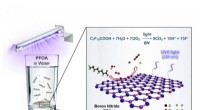
- Boornitride vernietigt voor altijd chemicaliën PFOA, GenX
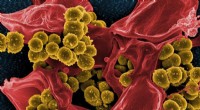
- Chemici ontwikkelen een nieuwe manier om antibioticaresistente infecties te behandelen
- Stress in kunststoffen visualiseren

- Studie onthult wetenschap achter traditionele techniek voor het maken van mezcal

- Metaalademende bacteriën kunnen elektronica transformeren, biosensoren, en meer

 Landen gaan aanzienlijke plastic bezuinigingen eens worden
Landen gaan aanzienlijke plastic bezuinigingen eens worden Kunnen we elders in het heelal leven?
Kunnen we elders in het heelal leven?  Onderzoek wijst op beleidsblauwdruk voor AI en machine learning
Onderzoek wijst op beleidsblauwdruk voor AI en machine learning Als een combinatiereactie plaatsvindt tussen kalium en chloor, wat is het product?
Als een combinatiereactie plaatsvindt tussen kalium en chloor, wat is het product?  Wat zijn planten met buisachtige structuren waardoor water en voedingsstoffen vanaf de wortels naar beneden kunnen reizen?
Wat zijn planten met buisachtige structuren waardoor water en voedingsstoffen vanaf de wortels naar beneden kunnen reizen?  Welk gezin bevat een volledig octet van valentie -elektronen?
Welk gezin bevat een volledig octet van valentie -elektronen?  Röntgenbeelden met een aanzienlijk verbeterde resolutie
Röntgenbeelden met een aanzienlijk verbeterde resolutie Wat zijn voorbeelden van mechanische verwering?
Wat zijn voorbeelden van mechanische verwering?
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

