
Wetenschap
Wat bedoel je met verbranding van een koolwaterstof?
Hier is een uitsplitsing:
* koolwaterstof: Dit is de brandstofbron. Voorbeelden zijn methaan (CH4), propaan (C3H8) en octaan (C8H18).
* zuurstof: Dit is de oxidatiemiddel, die nodig is om de reactie op te treden. Het is meestal uit de lucht gehaald.
* Warmte en licht: Dit zijn de producten van de reactie. De vrijgegeven energie maakt verbranding nuttig voor dingen als energiecentrales, motoren en open haarden.
De chemische reactie wordt in het algemeen weergegeven als:
Koolwaterstof + zuurstof → koolstofdioxide + water + warmte + licht
Bijvoorbeeld, de verbranding van methaan ziet er zo uit:
CH4 + 2O2 → CO2 + 2H2O + warmte + licht
Sleutelpunten over verbranding van koolwaterstof:
* exotherme reactie: Verbranding geeft warmte vrij, waardoor het een exotherme proces is.
* Volledige verbranding: Dit gebeurt wanneer er voldoende zuurstof is voor alle koolstof om in koolstofdioxide te veranderen (CO2).
* Onvolledige verbranding: Dit gebeurt wanneer er niet genoeg zuurstof is. Het produceert koolmonoxide (CO), een giftig gas.
* Toepassingen: Verbranding is cruciaal in veel industrieën en het dagelijks leven, waaronder:
* Power Generation
* Transport (interne verbrandingsmotoren)
* Verwarming
* Koken
Laat het me weten als je meer wilt weten over een specifiek aspect van koolwaterstofverbranding!
 Welke factoren hebben invloed op het smeltpunt?
Welke factoren hebben invloed op het smeltpunt?  Wat is de verzameling kleine waterdruppeltjes in de atmosfeer?
Wat is de verzameling kleine waterdruppeltjes in de atmosfeer?  Welk onderscheidend symbool wordt gebruikt om radioactieve materialen te identificeren?
Welk onderscheidend symbool wordt gebruikt om radioactieve materialen te identificeren?  Is het toevoegen van zout en azijn om een chemische reactie water te geven, kunt u de eenmaal terugnemen die het met gemaakte kristal eruit heeft gemengd?
Is het toevoegen van zout en azijn om een chemische reactie water te geven, kunt u de eenmaal terugnemen die het met gemaakte kristal eruit heeft gemengd?  Wat zijn wetenschappelijke methode -parameters?
Wat zijn wetenschappelijke methode -parameters?
 Reis om straling te controleren na het zinken van Russische onderzeeër in 1989
Reis om straling te controleren na het zinken van Russische onderzeeër in 1989 Verstikkende rook boven San Francisco zorgt voor vertragingen, sluitingen
Verstikkende rook boven San Francisco zorgt voor vertragingen, sluitingen Hoe een 1, 000 jaar oude tsunami in de Indische Oceaan wijst op groter risico dan aanvankelijk werd gedacht
Hoe een 1, 000 jaar oude tsunami in de Indische Oceaan wijst op groter risico dan aanvankelijk werd gedacht Studenten filmen adembenemende kromming van de aarde met behulp van een weerballon op grote hoogte
Studenten filmen adembenemende kromming van de aarde met behulp van een weerballon op grote hoogte De 20e eeuw was de heetste in bijna 2, 000 jaar, onderzoeken tonen aan
De 20e eeuw was de heetste in bijna 2, 000 jaar, onderzoeken tonen aan
Hoofdlijnen
- Wat zijn de vier delen van mitose?
- Waarom verteert het zoutzuur dat door de maag wordt geproduceerd zijn eigen slijmvliescellen?
- Hebben garnalen een zenuwstelsel?
- Hoe beïnvloeden de erfenis van bepaalde kenmerken van ouders en andere voorouders gedrag?
- Wie zijn de meest populaire wetenschapper?
- Wat is parasiet en geef voorbeelden?
- Hoe helpt de wetenschappelijke methode wetenschapper?
- Hoe zijn eetstokjes en wetenschap gerelateerd?
- Wat is een functie van het celmembraan in rode bloedcellen?
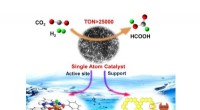
- Katalysator met één atoom gebaseerd op homogeen katalyse-prototype voor CO2-transformatie
- Actieve vloeibare kristalsystemen onderzocht op zoek naar autonome materiaalsystemen
- Nieuwe techniek bereidt 2-D perovskiet-eenkristallen voor voor de hoogste fotodetectie

- In-situ chemiestudies voor µSR

- Een kleine cirkelvormige racebaan voor licht kan snel afzonderlijke moleculen detecteren

 Plasticvervuiling:kunnen we de oceaan opruimen met technologie?
Plasticvervuiling:kunnen we de oceaan opruimen met technologie? Landingsplaats Mars 2020 biedt unieke kansen
Landingsplaats Mars 2020 biedt unieke kansen Lessen in voedselsystemen van COVID-19:van het begrijpen van kwetsbaarheden naar het opbouwen van veerkracht
Lessen in voedselsystemen van COVID-19:van het begrijpen van kwetsbaarheden naar het opbouwen van veerkracht Welk van dit element is niet essentieel voor levende organismen strontium zwavel natrium en selenium?
Welk van dit element is niet essentieel voor levende organismen strontium zwavel natrium en selenium?  Wetenschappers van de MAJORANA Collaboration zoeken naar elektronen die de regels overtreden
Wetenschappers van de MAJORANA Collaboration zoeken naar elektronen die de regels overtreden  Onderzoekers theoretiseren de oorsprong van magnetars, de sterkste magneten in het universum
Onderzoekers theoretiseren de oorsprong van magnetars, de sterkste magneten in het universum Welke van de volgende reacties toont dat de vorming SO2 296,8 kJ mol vrijgeeft?
Welke van de volgende reacties toont dat de vorming SO2 296,8 kJ mol vrijgeeft?  Zonne -huizen zonder speciale apparatuur om zonlicht te verzamelen?
Zonne -huizen zonder speciale apparatuur om zonlicht te verzamelen?
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

