
Wetenschap
Wat is de regel voor vervangingsreacties?
De regel voor vervangingsreacties:
Vervangende reacties, ook bekend als enkele verplaatsingsreacties , volg een eenvoudige regel:
Een meer reactief element zal een minder reactief element van de verbinding verplaatsen.
Hier is hoe het werkt:
1. reactanten: U begint met een element (A) en een verbinding (BC).
2. Reactiviteit: Het element (a) moet reactiever zijn dan het element (b) in de verbinding.
3. Verplaatsing: Het meer reactief element (a) zal het minder reactieve element (b) in de verbinding vervangen.
4. Producten: Dit resulteert in een nieuw element (B) en een nieuwe verbinding (AC).
Algemene formule:
A + BC → AC + B
Sleutelpunten:
* reactiviteitsreeks: De reactiviteit van elementen wordt bepaald door hun vermogen om elektronen te verliezen. Een reactiviteitreeks geeft elementen weer in volgorde van afnemende reactiviteit.
* Productie van producten: U kunt de reactiviteitsreeks gebruiken om de producten van een vervangingsreactie te voorspellen.
* Niet alle reacties treden op: Niet alle elementen zullen anderen uit hun verbindingen verplaatsen. Koper (Cu) is bijvoorbeeld minder reactief dan zilver (Ag), dus koper zal zilver niet uit zijn verbinding verplaatsen.
Voorbeelden:
* Zink reageert met zoutzuur: Zn + 2HCl → ZnCl2 + H2 (zink is meer reactief dan waterstof en verplaatst het uit zoutzuur)
* IJzer reageert met kopersulfaat: Fe + CUSO4 → FESO4 + Cu (ijzer is reactiever dan koper en verplaatst het van kopersulfaat)
Onthoud: Deze regel is van toepassing op zowel metalen als niet -metalen . De reactiviteitsreeks voor metalen en niet -metalen is echter anders.
 Waarom werd Darwins -theorie niet geaccepteerd?
Waarom werd Darwins -theorie niet geaccepteerd?  Ozongeneratoren kunnen helpen bij het oplossen van verontreiniging veroorzaakt door rook uit derdehands
Ozongeneratoren kunnen helpen bij het oplossen van verontreiniging veroorzaakt door rook uit derdehands Waarom slimme kraai geen vogelbrein is
Waarom slimme kraai geen vogelbrein is  Wat is de grootste menselijke impact op bosecosystemen?
Wat is de grootste menselijke impact op bosecosystemen?  Minstens 10 doden, 40 gewonden als aardbeving met 6,4 op het Indonesische eiland
Minstens 10 doden, 40 gewonden als aardbeving met 6,4 op het Indonesische eiland
Hoofdlijnen
- Waarom is de juiste microscooptechniek belangrijk voor het bestuderen van anatomie en fysiologie?
- Bloemstroken en heggen geven samen een boost aan bijen in boomgaarden
- Met behulp van nieuwe technieken doen onderzoekers verrassende ontdekkingen over hoe de hersenen van vliegen reageren op smaak
- Is het endoplasmatische reticuluum in planten- of dierlijke cel?
- Hoop op een van 's werelds zeldzaamste primaten:eerste telling van Zanzibar Red Colobus-aap
- Onderzoekers bieden visserij een oplossing voor overbevissing
- Waarom heeft het Digestif -systeem meer organen?
- De hoeveelheid organisch materiaal dat de autotrofe organismen een ecosysteem produceren?
- Is een lommerrijke zeedragon eukaryotisch of prokaryotisch?
- Onderzoek onthult hoe een klein molecuul de verwijdering van overtollig cholesterol bevordert
- Legeronderzoeker gebruikt wiskunde om nieuwe scheikunde te ontdekken

- Suiker aan eiwit plakken
- Gyroscoopmoleculen vormen kristal dat zowel solide als vol beweging is
- Biomimetische strategie leidt tot sterke, recyclebaar rubber
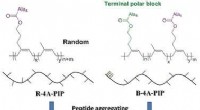
 Wat is het oxidatiegetal van calcium?
Wat is het oxidatiegetal van calcium?  Maangrot ontdekkingsreiziger
Maangrot ontdekkingsreiziger Waarom het bindende arbitragespel wordt opgetuigd tegen klanten?
Waarom het bindende arbitragespel wordt opgetuigd tegen klanten? Wiskundige strategieën voor kinderen met leerproblemen
Wiskundige strategieën voor kinderen met leerproblemen PaintBot:een diep lerende student die traint en vervolgens oude meesters nabootst
PaintBot:een diep lerende student die traint en vervolgens oude meesters nabootst Waarom zijn de onafhankelijke en afhankelijke variabelen belangrijk in een experiment?
Waarom zijn de onafhankelijke en afhankelijke variabelen belangrijk in een experiment?  Nieuwe lithografietechniek maakt de productie van nanoschaalpatronen van titania mogelijk voor hightech-toepassingen
Nieuwe lithografietechniek maakt de productie van nanoschaalpatronen van titania mogelijk voor hightech-toepassingen Kooldioxide katalyseren:systeem kan CO2 omzetten in CO voor gebruik in de industrie
Kooldioxide katalyseren:systeem kan CO2 omzetten in CO voor gebruik in de industrie
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

