
Wetenschap
Waarom gebruik je gesmolten NaCl in elektrolyse in plaats van een waterige oplossing NaCl?
gesmolten NaCl -elektrolyse:
* Product: Het primaire product is natriummetaal (NA) , wat een zeer reactief element is. Dit is niet mogelijk met een waterige oplossing omdat water zou reageren met het natrium.
* voorwaarden: Vereist hoge temperaturen (boven 801 ° C) om NaCl te smelten, wat energie -intensief is.
* nevenreacties: Geen, omdat er geen andere ionen aanwezig zijn behalve Na+ en Cl-.
* Toepassingen: Voornamelijk gebruikt bij de industriële productie van natriummetaal.
Waterige NaCl -elektrolyse:
* Producten: De producten zijn waterstofgas (H2) bij de kathode en chloorgas (CL2) bij de anode.
* voorwaarden: Kan worden gedaan bij kamertemperatuur en druk, veel energiezuiniger dan het gebruik van gesmolten zout.
* nevenreacties: Water wordt ook geëlektolyseerd, wat leidt tot de vorming van waterstof en zuurstof. Dit kan een gewenst of ongewenst product zijn, afhankelijk van de toepassing.
* Toepassingen: Gebruikt bij de productie van chloorgas en natriumhydroxide (NaOH), evenals in verschillende elektrochemische toepassingen.
Samenvattend:
* gesmolten NaCl: Gebruikt wanneer het primaire doel is om natriummetaal te produceren. Het is een gespecialiseerd proces met hoge energievereisten.
* waterige NaCl: Gebruikt wanneer het doel is om chloorgas, waterstofgas of natriumhydroxide te produceren. Dit is een meer gebruikelijk en veelzijdig proces.
De juiste methode kiezen:
De keuze van welke methode te gebruiken is afhankelijk van de gewenste producten. Als u natriummetaal wilt, moet u gesmolten NaCl gebruiken. Als u chloor of waterstof wilt, is een waterige oplossing efficiënter.
 Wat is het tegenovergestelde van gras?
Wat is het tegenovergestelde van gras?  Waar vindt Fotosynthese plaats in Mossen?
Waar vindt Fotosynthese plaats in Mossen?  Identiteitscrisis:klimaatvernietigende wonderen die Amerikaanse parken hun naam gaven
Identiteitscrisis:klimaatvernietigende wonderen die Amerikaanse parken hun naam gaven  Revenge of the seabed burrowers:een andere kijk op bioturbatie en oceaanecosystemen
Revenge of the seabed burrowers:een andere kijk op bioturbatie en oceaanecosystemen Nieuwe inzichten in de degradatiedynamiek van organisch materiaal in de zeebodem
Nieuwe inzichten in de degradatiedynamiek van organisch materiaal in de zeebodem
Hoofdlijnen
- 245 miljoen jaar oude fossielen bieden nieuwe inzichten in de evolutie en voedingsstrategieën van waterinsecten
- Haploid versus diploïde: wat zijn de overeenkomsten & verschillen?
- Wat is satelliet -DNA?
- Hoe lang geleden verschenen meercellige levensvormen in het fossiele record?
- Kun je organen zien met een microscoop?
- Hoe beïnvloedt een enzym een biologische reactie?
- Leg uit hoe de genetische code zowel continuïteit als verandering toont?
- Hoe verschilt de opperhuid van wortel van stam in structuur en functie?
- Welk deel van de dieren wordt zelden onbetoond omdat aaseters ze opeten en bacteriën ze ontcompeteren?
- Warmterecycling verbeteren met het thermodiffusie-effect

- Een milieuvriendelijkere airconditioner

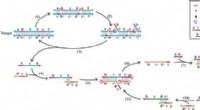
- Eenvoudig kopiëren:een universele isotherme DNA-amplificatiemethode
- Nieuwe manier om vloeibare druppels in te pakken kan de medicijnafgifte verbeteren

- Geïntegreerde waterstofopslag voor brandstofcelauto's

 Onderzoeksvraag:Is het veilig om mijn rekeningen via internet te betalen?
Onderzoeksvraag:Is het veilig om mijn rekeningen via internet te betalen?  Oud DNA laat zien dat de Sami en Finnen identieke Siberische genen delen
Oud DNA laat zien dat de Sami en Finnen identieke Siberische genen delen Purdue-startup wint Armys xTechZoek naar de nieuwste technologie om aan moderniseringsbehoeften te voldoen
Purdue-startup wint Armys xTechZoek naar de nieuwste technologie om aan moderniseringsbehoeften te voldoen Welke eigenschap wordt door Alchohal beschreven op 60 graden?
Welke eigenschap wordt door Alchohal beschreven op 60 graden?  Neutronen in cijfers:nieuwe teltechniek zorgt voor ongekende nauwkeurigheid
Neutronen in cijfers:nieuwe teltechniek zorgt voor ongekende nauwkeurigheid Paradijs herwonnen? Experts pleiten voor Europese aanpak van Amerikaanse huisvesting
Paradijs herwonnen? Experts pleiten voor Europese aanpak van Amerikaanse huisvesting Hoe botsende neutronensterren licht kunnen werpen op universele mysteries
Hoe botsende neutronensterren licht kunnen werpen op universele mysteries Een stap dichter bij milieuvriendelijke productie van waterstofbrandstof
Een stap dichter bij milieuvriendelijke productie van waterstofbrandstof
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

