
Wetenschap
Zou een ionische of covalente verbinding geleidender zijn in water wanneer opgelost, verklaren?
Verklaring:
* ionische verbindingen bestaan uit positief geladen ionen (kationen) en negatief geladen ionen (anionen) samengehouden door elektrostatische krachten. Wanneer opgelost in water, omringen de polaire watermoleculen de ionen, scheiden ze en laten ze vrij bewegen. Deze beweging van geladen deeltjes (ionen) creëert een elektrische stroom, waardoor de oplossing geleidelijk wordt.
* Covalente verbindingen worden gevormd door het delen van elektronen tussen atomen. Ze vormen geen ionen in oplossing, maar blijven eerder als neutrale moleculen. Aangezien er geen vrij bewegende geladen deeltjes zijn, leiden covalente verbindingen over het algemeen geen elektriciteit in water.
Belangrijkste verschillen:
| Feature | Ionische verbindingen | Covalente verbindingen |
| --- | --- | --- |
| Bonding | Elektrostatische krachten | Elektronen delen |
| Opgeloste soorten | Ionen | Moleculen |
| Geleidbaarheid | Hoog | Laag |
Voorbeelden:
* ionische verbinding: Natriumchloride (NaCl) lost in water op om Na+ en clies te vormen, waardoor de oplossing geleidelijk wordt.
* Covalente verbinding: Suiker (C12H22O11) lost op in water maar vormt geen ionen, dus de oplossing is niet geleidend.
Uitzonderingen:
Er zijn enkele uitzonderingen op deze algemene regel. Sommige covalente verbindingen, zoals zoutzuur (HCL), kunnen ioniseren in water en geleidend worden. Over het algemeen zijn ionische verbindingen echter aanzienlijk geleidender dan covalente verbindingen in water.
 Branden vormen de basis voor onomkeerbare bosverliezen in Australië
Branden vormen de basis voor onomkeerbare bosverliezen in Australië Braziliaanse rechtbank handhaaft grotendeels wet dat sommige angst Amazon pijn doet
Braziliaanse rechtbank handhaaft grotendeels wet dat sommige angst Amazon pijn doet Klimaatmodellen kunnen decadale regenvalvariaties op het Tibetaanse plateau voorspellen
Klimaatmodellen kunnen decadale regenvalvariaties op het Tibetaanse plateau voorspellen Regionale ongelijkheden binnen de EU zijn de afgelopen 35 jaar afgenomen
Regionale ongelijkheden binnen de EU zijn de afgelopen 35 jaar afgenomen Cryptozoology: The Pseudo-Science of Mythical Creatures
Cryptozoology: The Pseudo-Science of Mythical Creatures
Hoofdlijnen
- Cellen die ziekteverwekkers identificeren en van elkaar onderscheiden, wat wordt genoemd?
- Welk deel repliceert de celcyclus zijn DNA?
- Waarom komt evolutie voor door de overerving van verworven kenmerken?
- Welk monomeer wordt gevonden in amandelen maar geen RNA?
- Welk voedsel is geen functie-eiwit?
- Hoe wordt het genoemd als een cytoplasma begint te scheiden?
- Industrieel gebruik van Pepsin
- Hoe werd een eeuwenoude plant uit Latijns-Amerika het op een na belangrijkste marktgewas van Azië?
- Wat is de rol van enzymcomplex in de elektrontransportketen?
- Kunstmatige membraanbindende eiwitten om stamcellen naar het myocardium te leiden
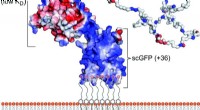
- Beoordeling van technologieën die het potentieel voor de omzetting van kooldioxide in bruikbare producten vergroten
- Coronavirus test vanuit een koffer
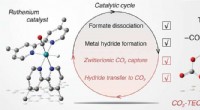
- Monitoring van tussenproducten in CO2-conversie naar formiaat door metaalkatalysator
- De oorsprong van smaakafwijkingen in uien
 Na de moord op Floyds, kinetische impactprojectielen bij protesten leidden tot meer dan 100 hoofdletsels
Na de moord op Floyds, kinetische impactprojectielen bij protesten leidden tot meer dan 100 hoofdletsels Wat begrijpt u bij Permuitit Hoe wordt uitgeput zeoliet geregenreerd?
Wat begrijpt u bij Permuitit Hoe wordt uitgeput zeoliet geregenreerd?  Handel in wilde dieren en meer belemmeren de duurzame ontwikkeling van landen
Handel in wilde dieren en meer belemmeren de duurzame ontwikkeling van landen Hoe ver moet een 100 Newton Force verhuizen om 1000 joules werk te doen?
Hoe ver moet een 100 Newton Force verhuizen om 1000 joules werk te doen?  Onderzoekers benutten methaanverbruikende microben voor gebruik in industriële toepassingen
Onderzoekers benutten methaanverbruikende microben voor gebruik in industriële toepassingen Is Earths Moon de enige die licht reflecteert?
Is Earths Moon de enige die licht reflecteert?  Koolstofnanostructuren groeien onder extreem deeltjesbombardement
Koolstofnanostructuren groeien onder extreem deeltjesbombardement Lithium-zwavelbatterijen gaan langer mee met kathode boordevol nanomateriaal
Lithium-zwavelbatterijen gaan langer mee met kathode boordevol nanomateriaal
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

