
Wetenschap
Reageren zink- en kopersulfaatoplossing?
Dit is waarom en wat er gebeurt:
* zink is reactiever dan koper. Dit betekent dat zink een sterkere neiging heeft om elektronen te verliezen en positieve ionen te vormen.
* Kopersulfaatoplossing bevat koperionen (Cu²⁺) en sulfaationen (So₄²⁻).
* Wanneer zink in de kopersulfaatoplossing wordt geplaatst, zullen de zinkatomen de koperionen uit de oplossing verplaatsen. Zinkatomen verliezen elektronen om zinkionen (Zn²⁺) te vormen, en de koperionen krijgen elektronen om koperatomen (Cu) te vormen.
De chemische vergelijking voor deze reactie is:
Zn (S) + Cuso₄ (aq) → ZnSo₄ (aq) + cu (s)
Dit is wat je zult waarnemen:
* een roodbruine vaste stof vormt zich op het oppervlak van het zink. Dit is het koper dat uit de oplossing wordt verplaatst.
* De blauwe kleur van de kopersulfaatoplossing zal geleidelijk vervagen. Dit komt omdat de koperionen uit de oplossing worden verwijderd.
Samenvattend zal de zink- en kopersulfaatoplossing reageren om zinksulfaatoplossing en koperen metaal te vormen. Deze reactie toont de relatieve reactiviteit van metalen.
 Wat is de naam van hij wetenschapper die ontdekte dat atomen positieve aanklacht hebben?
Wat is de naam van hij wetenschapper die ontdekte dat atomen positieve aanklacht hebben?  Waarom zijn alkaliën gevaarlijk?
Waarom zijn alkaliën gevaarlijk?  Een nieuwe manier om met zonlicht schone waterstofbrandstof te maken uit water
Een nieuwe manier om met zonlicht schone waterstofbrandstof te maken uit water Wetenschappers voorspellen nieuwe, moeilijk, en superharde ternaire verbindingen
Wetenschappers voorspellen nieuwe, moeilijk, en superharde ternaire verbindingen Hoe een Shell-model van calciumchloride te tekenen
Hoe een Shell-model van calciumchloride te tekenen
 Heeft het titaniumdioxide in voedsel en nanomaterialen invloed op het darmmicrobioom?
Heeft het titaniumdioxide in voedsel en nanomaterialen invloed op het darmmicrobioom? Wetenschappers ontdekken sleutelgen voor het produceren van mariene moleculen met enorme milieueffecten
Wetenschappers ontdekken sleutelgen voor het produceren van mariene moleculen met enorme milieueffecten Opsporen van subglaciale wateropslag
Opsporen van subglaciale wateropslag Sinabung in Indonesië spuwt kolom vulkanische as de lucht in
Sinabung in Indonesië spuwt kolom vulkanische as de lucht in Radarsatellieten kunnen beter beschermen tegen bosbranden en overstromingen
Radarsatellieten kunnen beter beschermen tegen bosbranden en overstromingen
Hoofdlijnen
- Zijn vissen de grootste atleten ter wereld?
- Goed excuus, of is er eigenlijk sprake van een vreemdgaan-gen?
- Welk lichaamssysteem heeft de grootste capaciteit voor pH -verandering in het lichaam?
- Aanvallen of terugtrekken? Circuit verbindt honger en achtervolging in de hersenen van zeeslakken
- Het menselijk brein is bedraad voor poëzie
- Wat is een knop en waar vormt deze op een organisme dat aseksueel reproduceert?
- Wat gebeurt er met je cellen als je gedehydrateerd bent?
- Welke term beschrijft de theorie dat leven voortkomt uit leven?
- Welk deel van de cel dient om pakket te verwerken en eiwitten te exporteren?
- Chemici stellen een nieuwe benadering voor van de synthese van het ABCD-ringsysteem van alpkinidine

- Een oplossing voor een harig probleem in de forensische wetenschap
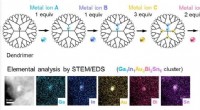
- Doorbraak in het mengen van metalen - nauwkeurige controle van multimetallische clustervorming van één nanometer bereikt
- Een nieuwe classificatie van symmetriegroepen in de kristalruimte voorgesteld door Russische wetenschappers
- Versneld klinisch gebruik van Raman-spectroscopie chemische vingerafdrukken

 Wat zijn de voordelen van HPLC over GC?
Wat zijn de voordelen van HPLC over GC?  Geef de biologische betekenis van celademhaling?
Geef de biologische betekenis van celademhaling?  De twee of meer gerelateerde genen die een eigenschap regelen, staan bekend als?
De twee of meer gerelateerde genen die een eigenschap regelen, staan bekend als?  Uit nieuw onderzoek blijkt dat we duurzaamheid serieus nemen, maar dat we niet weten wat onze acties waard zijn
Uit nieuw onderzoek blijkt dat we duurzaamheid serieus nemen, maar dat we niet weten wat onze acties waard zijn  Vervuiling van uitlaatgassen van raketmotoren breidt zich uit tot diep in de atmosfeer van de aarde
Vervuiling van uitlaatgassen van raketmotoren breidt zich uit tot diep in de atmosfeer van de aarde Kubieke voetjes in een kegelvorm tekenen
Kubieke voetjes in een kegelvorm tekenen  Wat concludeerde Galileo uit zijn observaties van Jupiter en Venus?
Wat concludeerde Galileo uit zijn observaties van Jupiter en Venus?  Waarom vertrouwen we op onze vijf zintuigen om het weer te beschrijven en te meten?
Waarom vertrouwen we op onze vijf zintuigen om het weer te beschrijven en te meten?
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

