
Wetenschap
Welke soorten intermoleculaire krachten kunnen er bestaan tussen jodium van moleculen?
Dit is waarom:
* jodium is niet -polair: Het I₂ -molecuul is symmetrisch, met de elektronen gelijkmatig verdeeld. Dit betekent dat het geen permanent dipoolmoment heeft.
* LDF's komen voort uit tijdelijke dipolen: Hoewel jodium niet -polair is, zijn de elektronen constant in beweging. Op elk gegeven moment kan er een tijdelijke onbalans in elektronenverdeling zijn, waardoor een tijdelijke, onmiddellijke dipool ontstaat. Deze tijdelijke dipool kan vervolgens een tijdelijke dipool induceren in een aangrenzend jodiummolecuul. Deze zwakke, tijdelijke attracties zijn LDF's.
Hoewel jodium ook dipool-geïnduceerde dipoolkrachten kan ervaren, zijn deze aanzienlijk zwakker dan LDF's vanwege het gebrek aan permanente dipolen.
Samenvattend is de dominante intermoleculaire kracht in jodium London Dispersion Forces (LDFS).
Hoofdlijnen
- Hoe planten microben benutten om voedingsstoffen binnen te krijgen
- Wat zijn leden van een groep die kan worden geroepen?
- Welke hormonen produceert de hypofyse?
- Leeftijd van moeders beïnvloedt genetische overeenkomst tussen tweelingen
- Welk type zenuw ontvangt stimuli uit de omgeving en verzendt bericht naar de hersenen?
- Oud skelet onthult amputatie-operatie 31.000 jaar geleden
- Milieu op basis van evolutie indelen in twee categorieën?
- Zeldzame trofische eieren achter het succes van slangenkopvissen?
- Als ribosomen botsen:hoe bacteriën opruimen na moleculaire crashes
- Ontwerpen van de volgende generatie haarkleurmiddelen

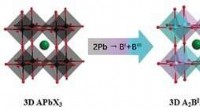
- Onderzoekers ontwikkelen halide dubbele perovskiet ferro-elektriciteit
- Zeesponzen blijven zitten met ankers die buigen maar niet breken

- Een herbruikbare katalysator voor de synthese van esters
- Een effectieve manier om atrazin en zijn bijproducten in oppervlaktewater te elimineren

 Waarom begon Mendel zijn experimenten door eren te laten pollineren voor meerdere generaties?
Waarom begon Mendel zijn experimenten door eren te laten pollineren voor meerdere generaties?  Heeft het zijn smaak behouden? Kauwgom uit het stenen tijdperk levert menselijk DNA op
Heeft het zijn smaak behouden? Kauwgom uit het stenen tijdperk levert menselijk DNA op Hoe is het klimaat gekoppeld aan de bodemkwaliteit?
Hoe is het klimaat gekoppeld aan de bodemkwaliteit?  Vraag van $500 miljard:wat is de waarde van het bestuderen van de biologische koolstofpomp van de oceaan?
Vraag van $500 miljard:wat is de waarde van het bestuderen van de biologische koolstofpomp van de oceaan?  Wat orkanen betekenen voor Red Tide
Wat orkanen betekenen voor Red Tide Hoe wetenschappers over de hele wereld de zonnecyclus volgen
Hoe wetenschappers over de hele wereld de zonnecyclus volgen  Een structurele lichtschakelaar voor magnetisme
Een structurele lichtschakelaar voor magnetisme Gecontroleerde en gerichte afgifte van medicijnen
Gecontroleerde en gerichte afgifte van medicijnen
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com


