
Wetenschap
Wordt een compound bij elkaar gehouden door tegengestelde aanklachten?
Hier is hoe het werkt:
* ionische bindingen Vorm wanneer één atoom verliest Elektronen (positief geladen worden, een kation genoemd ) en een ander atoom wint Die elektronen (negatief geladen worden, een anion genoemd ).
* De tegenovergestelde ladingen tussen het kation en het anion creëren een sterke elektrostatische aantrekkingskracht, die ze bij elkaar houdt in een verbinding .
Bijvoorbeeld:
* Natrium (NA) verliest één elektron om een positief geladen natriumion (Na+) te worden.
* Chloor (CL) wint dat elektron om een negatief geladen chloride-ion te worden (Cl-).
* De tegenovergestelde ladingen tussen Na+ en Cl-aantrekken, die het ionische samengestelde natriumchloride (NaCl) vormen- tafelzout.
Belangrijke opmerking: Niet alle verbindingen worden bij elkaar gehouden door ionische bindingen. Covalente bindingen, waar atomen elektronen delen, zijn ook een veel voorkomend type chemische binding. Het principe van tegengestelde ladingen is echter nog steeds op een andere manier van toepassing op covalente bindingen, omdat elektronen worden gedeeld tussen atomen met verschillende elektronegativiteiten, wat resulteert in een gedeeltelijke positieve en negatieve lading op elk atoom.
 Wat is het verschil tussen een stikstofatoom N en ion N3?
Wat is het verschil tussen een stikstofatoom N en ion N3?  Maakt platina geluid als je erop slaat?
Maakt platina geluid als je erop slaat?  Nieuw fluorescentiedetectieplatform ontwikkeld voor visuele monitoring van voedselveiligheid
Nieuw fluorescentiedetectieplatform ontwikkeld voor visuele monitoring van voedselveiligheid Een nieuwe manier om hout transparant te maken, sterker en lichter dan glas
Een nieuwe manier om hout transparant te maken, sterker en lichter dan glas Doorbraak in magnesiumbatterijen:nanogestructureerde kathode, begrip van nieuwe elektrolyt leidt tot grotere efficiëntie
Doorbraak in magnesiumbatterijen:nanogestructureerde kathode, begrip van nieuwe elektrolyt leidt tot grotere efficiëntie
 Hoe beïnvloeden mensen het milieu Portugal?
Hoe beïnvloeden mensen het milieu Portugal?  Wat is de sleutel tot natuurlijke selectie?
Wat is de sleutel tot natuurlijke selectie?  Onderzoekers lokaliseren oorzaak van dodelijke muistroom in Lake Michigan
Onderzoekers lokaliseren oorzaak van dodelijke muistroom in Lake Michigan De grootste massa-extinctie op aarde duurde tien keer langer op het land dan in het water
De grootste massa-extinctie op aarde duurde tien keer langer op het land dan in het water 'S Werelds grootste opiniepeiling over klimaatverandering:meerderheid roept op tot brede actie
'S Werelds grootste opiniepeiling over klimaatverandering:meerderheid roept op tot brede actie
Hoofdlijnen
- Wat verklaarde Lynn Margulis de aanwezigheid van DNA in chromatine en chromosomen?
- Wat is het verschil tussen conjugatie die optreedt bij paramecia en bacteriën?
- Wat is de algemene term voor single genaamd organismen met kern?
- Zijn mannen of vrouwen gelukkiger?
- Hoe lossen we het probleem van de afvoer van nutriënten in de landbouw op?
- Bacteriën coderen voor verborgen genen buiten hun genoom; wij?
- De drie dingen die de plant binnenkomen tijdens fotosynthese zijn?
- Wat betekent deamatologie?
- Wat is grasbankieren?
- Atomaire vingerafdruk identificeert emissiebronnen van uranium

- Technische defecten in kristallijn materiaal verhogen de elektrische prestaties

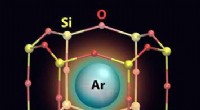
- Bestuderen van argongas gevangen in een tweedimensionale reeks kleine kooien
- Nieuwe methode voor het produceren van synthetisch DNA
- Computationele tools en nieuwe strategieën maken het ontdekken van medicijnen efficiënter

 Ruimtetechnologie voorspelt droogtes enkele maanden van tevoren
Ruimtetechnologie voorspelt droogtes enkele maanden van tevoren Welke is de kracht van afstoting tussen twee positief geladen deeltjes?
Welke is de kracht van afstoting tussen twee positief geladen deeltjes?  Welke ster produceert alle elementen van helium door ijzer?
Welke ster produceert alle elementen van helium door ijzer?  Wat is de naam van Astronut die de meeste tijd in de ruimte heeft doorgebracht?
Wat is de naam van Astronut die de meeste tijd in de ruimte heeft doorgebracht?  Hoeveel vierkante gevoel is 115 inch bij 2 voet?
Hoeveel vierkante gevoel is 115 inch bij 2 voet?  Histogramkenmerken
Histogramkenmerken Welke theorieën geloofden oude wetenschappers vóór de celtheorie?
Welke theorieën geloofden oude wetenschappers vóór de celtheorie?  Wat is een voorspelbare voorspelling?
Wat is een voorspelbare voorspelling?
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

