
Wetenschap
Welke verbinding is kleurloos in een wateroplossing Al2SO43 Cr2SO43 Fe2SO43 CO2SO43?
* Kleur begrijpen in oplossingen: Overgangsmetaalionen (elementen in het D-blok van de periodieke tabel) vormen vaak gekleurde oplossingen vanwege de absorptie en emissie van licht wanneer elektronen tussen energieniveaus overgaan.
* De verbindingen:
* al₂ (So₄) ₃: Aluminium (AL) is een groep 3 -element, geen overgangsmetaal. De ionen zijn meestal kleurloos.
* cr₂ (So₄) ₃: Chroom (CR) is een overgangsmetaal. Chroom (III) ionen (cr³⁺) staan bekend om hun groene kleur in oplossing.
* fe₂ (So₄) ₃: IJzer (Fe) is een overgangsmetaal. IJzer (III) ionen (Fe³⁺) kunnen gele tot roodbruine oplossingen vormen.
* co₂ (So₄) ₃: Kobalt (CO) is een overgangsmetaal. Kobalt (II) ionen (co²⁺) zijn meestal roze of blauw in oplossing, en kobalt (III) ionen (co³⁺) kunnen verschillende kleuren zijn, afhankelijk van de ligandcoördinatie.
Conclusie:
Daarom is de verbinding die kleurloos is in een wateroplossing al₂ (SO₄) ₃ .
 Wat is de massa van 175 atomen goud?
Wat is de massa van 175 atomen goud?  Hoeveel atomen zijn er in lachinggas?
Hoeveel atomen zijn er in lachinggas?  Wanneer een neutraal atoom zo'n kalium 1 elektron verliest, wordt zijn lading welk nummer?
Wanneer een neutraal atoom zo'n kalium 1 elektron verliest, wordt zijn lading welk nummer?  Nieuwe methode gebruikt kunstmatige intelligentie om levende cellen te bestuderen
Nieuwe methode gebruikt kunstmatige intelligentie om levende cellen te bestuderen Een hoog gehalte aan triethylfosfaat gebaseerde, niet-ontvlambare en hooggeleidende elektrolyt voor lithium-ionbatterijen
Een hoog gehalte aan triethylfosfaat gebaseerde, niet-ontvlambare en hooggeleidende elektrolyt voor lithium-ionbatterijen
 Verschillen tussen een zure wasmiddelvezel en een neutrale detergent Fiber
Verschillen tussen een zure wasmiddelvezel en een neutrale detergent Fiber De leeftijd van de binnenkern van de aarde herzien
De leeftijd van de binnenkern van de aarde herzien Kaarten ontwikkeld met kunstmatige intelligentie bevestigen lage fosforniveaus in de bodem van het Amazonegebied
Kaarten ontwikkeld met kunstmatige intelligentie bevestigen lage fosforniveaus in de bodem van het Amazonegebied  Hoe klimaatverandering de dennenplantages kan hervormen
Hoe klimaatverandering de dennenplantages kan hervormen Wat gebeurt er als u bomen blijft kappen?
Wat gebeurt er als u bomen blijft kappen?
Hoofdlijnen
- Wat heeft meer biomassa voor fotosynthetisch weefsel en minder ondersteunend weefsel?
- Als het gaat om hoe pizza eruit ziet, is kaas belangrijk
- Ziet DNA er hetzelfde uit in elk organisme?
- Waarom worden ze lagere dieren genoemd?
- Welke stap van de wetenschappelijke methode omvat het identificeren van variabelen?
- Wat is het verschil tussen stratum germinativum en basale?
- Drie decennia van onderzoek mondt uit in meer unieke orchideeënsoorten
- Een sekseverschil in sportinteresse:wat zegt de evolutie?
- Protoplasma is al het levende materiaal waar?
- CO2-uitstoot opruimen kan miljoenen waard zijn

- Nieuw ontwikkelde molecule om geneesmiddelen te verbeteren, haalt inspiratie uit de gereedschapskist van de natuur

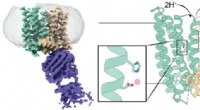
- Onthulling van de onverwachte structuur van ijzer-exporteur ferroportine
- Knoeien met cellulaire vetten is veelbelovend

- snel, flexibele wateranalyse zorgt voor opschudding in de industrie

 Welke eigenschappen van lucht produceren een dunderingsrom?
Welke eigenschappen van lucht produceren een dunderingsrom?  Hoe zouden de bijna Tsky eruit zien als All-Stars dezelfde absolute omvang hadden als zon?
Hoe zouden de bijna Tsky eruit zien als All-Stars dezelfde absolute omvang hadden als zon?  Berekening van de warmtecapaciteit
Berekening van de warmtecapaciteit Als je goed keek, zou je de golflengte van een snel bewegende auto kunnen zien?
Als je goed keek, zou je de golflengte van een snel bewegende auto kunnen zien?  Wat voor soort reactie is azijnzuur plus kaliumhydroxide?
Wat voor soort reactie is azijnzuur plus kaliumhydroxide?  Onderzoekers bereiken een kwantumopbrengst van 99% fotoluminescentie in metalen nanoclusters
Onderzoekers bereiken een kwantumopbrengst van 99% fotoluminescentie in metalen nanoclusters  De overdracht van warmte door middel van stralen?
De overdracht van warmte door middel van stralen?  Wat zijn slechte dingen over de wetenschap?
Wat zijn slechte dingen over de wetenschap?
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

