
Wetenschap
Welke oplossing produceert het meest waarschijnlijk kristallen als deze wordt gestoord?
Dit is waarom en wat we moeten overwegen:
* Samenstelling van oplossingen: Het type opgeloste stof (de stof die wordt opgelost) en het oplosmiddel (de stof die het oplost) is cruciaal. Oplossingen van zouten zoals suiker of tafelzout hebben bijvoorbeeld meer kans om te kristalliseren dan oplossingen van organische moleculen zoals alcohol of azijn.
* concentratie: Een oververzadigde oplossing (meer opgeloste stof vasthouden dan normaal bij een gegeven temperatuur) is veel meer kans om te kristalliseren dan een verdunde oplossing.
* Temperatuur: Het koelen van een oplossing kan er vaak toe leiden dat deze oververzadigd wordt en de kans op kristallisatie vergroten.
* nucleatie -sites: Verstoringen introduceren onvolkomenheden of "zaden" die kunnen fungeren als nucleatieplaatsen, waar kristallen beginnen te vormen.
Voorbeelden:
* oververzadigde suikeroplossing: Als u een oververzadigde suikeroplossing schudt, ziet u waarschijnlijk de kristallen snel vormen.
* Rock Candy: Een oververzadigde suikeroplossing wordt opzettelijk gestoord door een touwtje toe te voegen of stick toe te voegen om kristalgroei te bevorderen.
* Zoutoplossing: Een verzadigde zoutoplossing kan in de loop van de tijd langzaam kristalliseren, maar het storen kan snellere kristallisatie aanmoedigen.
Geef om een beter antwoord te krijgen, geef meer informatie over de oplossing waarin u geïnteresseerd bent!
 Wat kan verschillende fasen van het atoom zien?
Wat kan verschillende fasen van het atoom zien?  Waarom vindt er geen kleurverandering plaats als waterstofperoxide en kaliumjodide reageren?
Waarom vindt er geen kleurverandering plaats als waterstofperoxide en kaliumjodide reageren?  Gebruik maken van de slagvastheid van 's werelds hardste beton voor rampenpreventie
Gebruik maken van de slagvastheid van 's werelds hardste beton voor rampenpreventie Gespecialiseerde structuren die gas kunnen binnenkomen en blad verlaten?
Gespecialiseerde structuren die gas kunnen binnenkomen en blad verlaten?  Kan een stof zowel in vet oplosbaar als in water oplosbaar zijn?
Kan een stof zowel in vet oplosbaar als in water oplosbaar zijn?
 Wetenschappers synthetiseren onderzoek, model voor kustbepantsering evalueren
Wetenschappers synthetiseren onderzoek, model voor kustbepantsering evalueren Kan de grootste boosdoener van de opwarming van de aarde de gewassen helpen?
Kan de grootste boosdoener van de opwarming van de aarde de gewassen helpen?  NASA's Terra Satellite vindt krachtige stormen in orkaan Hector
NASA's Terra Satellite vindt krachtige stormen in orkaan Hector Internationaal ozonverdrag stopt veranderingen in winden op zuidelijk halfrond
Internationaal ozonverdrag stopt veranderingen in winden op zuidelijk halfrond NASA-satelliet ziet branden in het zuidoosten van de VS
NASA-satelliet ziet branden in het zuidoosten van de VS
Hoofdlijnen
- Welke radioactieve tracer verscheen in de bacteriën die Hershey leidden en achtervolgde tot hun conclusie DNA niet eiwit was genetisch materiaal?
- Hoe planten reageren op hittestress
- Welk woord is Quackenbush dat ervoor zorgt dat Gene vecht?
- AI-aangedreven virtuele rat biedt inzicht in hoe hersenen complexe, gecoördineerde bewegingen controleren
- Wat zijn weefsels in de huid?
- Een schakelaar voor de interne klok:onderzoek naar kwantumbiologie voor nieuwe medische therapieën
- Waarom de suikerkorrels een monster van de materie zijn. Welke reden?
- Hoe lijken mitochondriën en chloroplasten op bacteriën?
- Wie stelde het idee van overleven die fittest is een theorie -evolutie voor?
- Onderzoekers ontdekken verborgen SARS-CoV-2-poort die opengaat om COVID-infectie mogelijk te maken

- Wetenschappers ontwikkelen moleculaire code voor melanine-achtige materialen

- Ultragevoelige toxische gasdetector

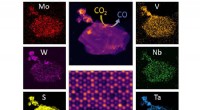
- Nieuwe 2D-legering combineert vijf metalen, breekt koolstofdioxide af
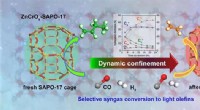
- Dynamische opsluiting van SAPO-17-kooien op selectiviteitscontrole van syngasconversie
 Kippen, eenden, zeehonden en koeien:een gevaarlijke vogelgriepstam klopt op de deur van Australië
Kippen, eenden, zeehonden en koeien:een gevaarlijke vogelgriepstam klopt op de deur van Australië  Welke eigenschappen heeft de zon gemeen met andere sterren?
Welke eigenschappen heeft de zon gemeen met andere sterren?  Target bestrijdt Amazon door gratis verzending binnen twee dagen aan te bieden en online bestellingen naar auto's te brengen
Target bestrijdt Amazon door gratis verzending binnen twee dagen aan te bieden en online bestellingen naar auto's te brengen Hoe worden magnetrons uit de ruimte gedetecteerd en wat vertellen ze ons over het begin van het universum?
Hoe worden magnetrons uit de ruimte gedetecteerd en wat vertellen ze ons over het begin van het universum?  Projecten voor 5e nivelleermachines om te doen over de watercyclus
Projecten voor 5e nivelleermachines om te doen over de watercyclus  Toenemende trends van warme en natte extremen vertraagden in China tijdens de recente onderbreking van de opwarming van de aarde
Toenemende trends van warme en natte extremen vertraagden in China tijdens de recente onderbreking van de opwarming van de aarde Wat is het belang van kleine anorganische zouten voor levende organismen?
Wat is het belang van kleine anorganische zouten voor levende organismen?  Wat betekent oplossing in de wetenschap?
Wat betekent oplossing in de wetenschap?
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

