
Wetenschap
Heeft koolstof meer atomaire straal dan germanium?
Dit is waarom:
* Atomaire maat trend: Atomische straal neemt in het algemeen toe naarmate u een groep in het periodiek systeem naar beneden verplaatst. Dit komt omdat het aantal elektronenschalen toeneemt, wat leidt tot een groter atoom.
* Positie: Koolstof en Germanium zijn beide in groep 14 (ook bekend als groep IV) van de periodiek systeem. Germanium bevindt zich onder koolstof, wat betekent dat het meer elektronenschalen heeft.
* Afschermingseffect: De extra elektronenschalen in Germanium verhogen ook het afschermingseffect, waarbij binnenste elektronen de buitenste elektronen beschermen tegen de aantrekkelijke kracht van de kern. Dit draagt verder bij aan een grotere atoomradius.
Daarom heeft Germanium een grotere atoomradius dan koolstof.
 Welke van de fluoriden zijn onoplosbaar?
Welke van de fluoriden zijn onoplosbaar?  Wetenschappers produceren hoogwaardig gips volledig uit afval
Wetenschappers produceren hoogwaardig gips volledig uit afval Wat is de ductiliteit van chloor?
Wat is de ductiliteit van chloor?  Wat zijn de zes ionen met dezelfde elektronenconfiguratie als Ne?
Wat zijn de zes ionen met dezelfde elektronenconfiguratie als Ne?  Wat is de verandering in energie AE kilojoule per mol waterstofatomen voor een elektronenovergang van N6 naar N2?
Wat is de verandering in energie AE kilojoule per mol waterstofatomen voor een elektronenovergang van N6 naar N2?
 Klimaatverandering:waarom we niet kunnen vertrouwen op het hergroeien van kusthabitats om de CO2-uitstoot te compenseren
Klimaatverandering:waarom we niet kunnen vertrouwen op het hergroeien van kusthabitats om de CO2-uitstoot te compenseren  NASA analyseerde de intensivering van de regens van Franklins voordat ze aan land kwamen
NASA analyseerde de intensivering van de regens van Franklins voordat ze aan land kwamen Magnetisme van Himalaya-rotsen onthult de complexe tektonische geschiedenis van de bergen
Magnetisme van Himalaya-rotsen onthult de complexe tektonische geschiedenis van de bergen Hoe een poging om het gebruik van fossiele brandstoffen te verminderen tot een ander milieuprobleem leidde:lichtvervuiling
Hoe een poging om het gebruik van fossiele brandstoffen te verminderen tot een ander milieuprobleem leidde:lichtvervuiling Indië, Nepal meest blootgesteld aan hoge concentraties vervuiling
Indië, Nepal meest blootgesteld aan hoge concentraties vervuiling
Hoofdlijnen
- Wat is een definitie van ecologische onbalans?
- Welke planten zitten in de maïsfamilie?
- Waarom enzymen worden hydrolytische enzymen genoemd?
- Wat is de naam voor een groep cellen die samenwerkt om een bepaalde taak uit te voeren in het N -organisme?
- Wat is het meest complex?
- Welk bioom bevat planten en dieren die zijn aangepast om water te besparen?
- Welke oplossing veroorzaakt niet de netto beweging van water in of uit een rode bloedcel?
- Wat is osmoregulatie en waarom is het belangrijk in levende organismen?
- Waarom kun je zeggen dat biologie leven en biologie is?
- Loodhalogenide perovskieten:een paard met een andere kleur

- Nieuwe NMR-techniek biedt moleculair inzicht in levende organismen

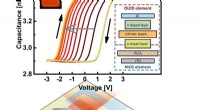
- pinMOS:nieuw geheugenapparaat kan optisch of elektrisch worden beschreven en uitgelezen
- ARS Cotton Advance helpt bij het lanceren van wondverband

- Bioplottering van bot-mimetische 3D-weefselsteigers met osteogene effecten

 Wat kunt u doen om energie te besparen?
Wat kunt u doen om energie te besparen?  Bosverlies hotspots groter dan Duitsland:WWF
Bosverlies hotspots groter dan Duitsland:WWF Definitie van Math Anxiety
Definitie van Math Anxiety Hoeveel worden astronomen in een jaar betaald?
Hoeveel worden astronomen in een jaar betaald?  Wat is een levenscyclus van een planten?
Wat is een levenscyclus van een planten?  Nieuwe katalysatorstrategie biedt oplossing voor efficiënte CO₂-reductiereactie
Nieuwe katalysatorstrategie biedt oplossing voor efficiënte CO₂-reductiereactie  Studie:Twijfels over ISO 9001-kwaliteitscertificaten van Chinese bedrijven
Studie:Twijfels over ISO 9001-kwaliteitscertificaten van Chinese bedrijven Vuur in de ruimte-experiment begint aan boord van Amerikaans vrachtschip (update)
Vuur in de ruimte-experiment begint aan boord van Amerikaans vrachtschip (update)
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

