
Wetenschap
Wat gebeurt er wanneer meng water met ionische oplossing?
1. Verdunning: De ionische oplossing wordt minder geconcentreerd. De ionen uit de oplossing zijn nu verspreid in een groter volume water.
2. Dissociatie: Als de ionische oplossing nog niet volledig is gedissocieerd, kunnen de watermoleculen de ionische verbinding in zijn samenstellende ionen verder breken. Dit komt door de polaire aard van watermoleculen, die kunnen interageren met en de geladen ionen kunnen omringen.
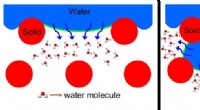
3. Hydratatie: De watermoleculen omringen de ionen en vormen een hydratatieschaal. Deze interactie helpt de ionen in oplossing te stabiliseren en te voorkomen dat ze recombineren.
4. Geleidbaarheid: De oplossing wordt elektrisch geleidend. De aanwezigheid van vrij bewegende ionen zorgt voor de stroom van elektrische stroom.
5. Colligatieve eigenschappen: De toevoeging van opgeloste stof (de ionische verbinding) kan de colligatieve eigenschappen van de oplossing beïnvloeden. Deze omvatten:
* dampdrukverlaging: De dampdruk van de oplossing neemt af in vergelijking met zuiver water.
* Kookpunthoogte: Het kookpunt van de oplossing neemt toe in vergelijking met zuiver water.
* Freezing Point Depression: Het vriespunt van de oplossing neemt af in vergelijking met zuiver water.
* osmotische druk: De oplossing ontwikkelt een osmotische druk, wat de druk is die nodig is om de stroom van water over een semipermeabiel membraan te voorkomen.
Voorbeeld:
Laten we een voorbeeld nemen van het oplossen van natriumchloride (NaCl) in water.
* dissociatie: NaCl dissocieert in Na+ en clies in water.
* Hydratatie: Watermoleculen omringen de Na+ en clies en vormen hydratatieschelpen.
* geleidbaarheid: De oplossing wordt geleidend vanwege de aanwezigheid van vrij bewegende ionen.
* Colligatieve eigenschappen: Het kookpunt van de oplossing neemt toe, het vriespunt neemt af en de dampdruk is lager dan zuiver water.
Over het algemeen: Het mengen van water met een ionische oplossing resulteert in een oplossing die minder geconcentreerd is, vrij bewegende ionen bevat en veranderde colligatieve eigenschappen vertoont.
 Chemicus maakt de volgende generatie neurowetenschappelijke tools
Chemicus maakt de volgende generatie neurowetenschappelijke tools Veiligheidsmaatregelen bij het gebruik van vlammen in de wetenschap
Veiligheidsmaatregelen bij het gebruik van vlammen in de wetenschap  Wat doen moleculen altijd?
Wat doen moleculen altijd?  Als een zaadkristal aan de oververzadigde oplossing werd toegevoegd, hoe zou u de resulterende oplossing karakteriseren?
Als een zaadkristal aan de oververzadigde oplossing werd toegevoegd, hoe zou u de resulterende oplossing karakteriseren?  Als je naar het etiket op een fles zuur kijkt, hoe kun je dan zien of het geconcentreerd is of niet?
Als je naar het etiket op een fles zuur kijkt, hoe kun je dan zien of het geconcentreerd is of niet?
 Oceaan circulatie, in combinatie met veranderingen in de passaatwind, beperkt efficiënt de verschuiving van tropische regenvalpatronen
Oceaan circulatie, in combinatie met veranderingen in de passaatwind, beperkt efficiënt de verschuiving van tropische regenvalpatronen Satellietanalyse onthult en asymmetrische Typhoon Bualoi
Satellietanalyse onthult en asymmetrische Typhoon Bualoi Wat is de vrijetijdsbosstatus?
Wat is de vrijetijdsbosstatus?  NASA's Aqua Satellite vindt een groot haveloos oog in tyfoon Krosa
NASA's Aqua Satellite vindt een groot haveloos oog in tyfoon Krosa Een punt van land dat in een lichaamswater reikt?
Een punt van land dat in een lichaamswater reikt?
Hoofdlijnen
- Hoe vaak zijn er meerdere organismen geëvolueerd uit unicells?
- Een plaag van onze eigen makelij:het onthullen van de ware oorsprong van de niet zo Duitse kakkerlak
- Wat heeft de biosfeer gemeen met een aquarium?
- Ben jij een zoetekauw? Honingbijen klauwen
- De donkergekleurde ronde structuur in de kern staat bekend als?
- Kunnen honden de bron zijn van een nieuwe griep?
- Hoe werken de structuren in een dierencel?
- Deze kleine ouders van koraalrifvissen beslissen wanneer hun embryo's uitkomen
- Hoe bavianen gezonde gezinsgrenzen bewaren
- Metaalademende bacteriën kunnen elektronica transformeren, biosensoren, en meer

- Wetenschappers onthullen belangrijke inzichten in opkomende waterzuiveringstechnologie
- Video:Hoe communiceren planten met elkaar?

- San Antonio-onderzoekers proberen storingen in de ruimtevaart en rampen met olielozingen te voorkomen

- Nieuw proces stimuleert lignine bio-olie als brandstof van de volgende generatie

 EU-boete op Google weegt op winst van moedermaatschappij Alphabet
EU-boete op Google weegt op winst van moedermaatschappij Alphabet Wie zal de slee van de Kerstman leiden terwijl de rendieren achteruitgaan?
Wie zal de slee van de Kerstman leiden terwijl de rendieren achteruitgaan?  Welke koninkrijken bevatten heterotrofe organismen?
Welke koninkrijken bevatten heterotrofe organismen?  Hoe erfelijke ziekten werken
Hoe erfelijke ziekten werken  Nieuw biomateriaal kan plastic laminaten vervangen, sterk verminderen vervuiling
Nieuw biomateriaal kan plastic laminaten vervangen, sterk verminderen vervuiling Roadmap-lekken laten de comeback-poging van BlackBerry zien
Roadmap-lekken laten de comeback-poging van BlackBerry zien  Onderzoekers beschrijven hoe cellen het afval buiten zetten om ziekten te voorkomen
Onderzoekers beschrijven hoe cellen het afval buiten zetten om ziekten te voorkomen  Mensen gaan ervan uit dat ze immuun zijn voor de dynamiek van sociale netwerken, maar andere mensen niet
Mensen gaan ervan uit dat ze immuun zijn voor de dynamiek van sociale netwerken, maar andere mensen niet
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

