
Wetenschap
Welk type binding heeft N2?
N2 (stikstofgas) heeft een drievoudige covalente binding .
Dit is waarom:
* Elektronenconfiguratie van stikstof: Elk stikstofatoom heeft 5 valentie -elektronen. Om een stabiele octetconfiguratie te bereiken, heeft deze nog 3 elektronen nodig.
* Elektronen delen: Stikstofatomen delen elk drie elektronen en vormen een drievoudige binding (drie paar gedeelde elektronen). Dit resulteert in elk stikstofatoom met 8 elektronen in zijn buitenste schaal, waardoor de octetregel wordt vervuld.
De drievoudige binding in N2 maakt het erg sterk en stabiel, daarom is stikstofgas onder normale omstandigheden zo niet -reactief.
 Universele latente aniondonoren voor ultralage werkfunctie-oplossing-verwerkbare elektroden
Universele latente aniondonoren voor ultralage werkfunctie-oplossing-verwerkbare elektroden Experimenten met zout en azijn
Experimenten met zout en azijn  Stappen in het vinden van percentagerendement
Stappen in het vinden van percentagerendement Nieuw superomnifoob glas zweeft hoog op vlindervleugels met behulp van machine learning
Nieuw superomnifoob glas zweeft hoog op vlindervleugels met behulp van machine learning Zijn ammoniumsulfaat en aluminium hetzelfde?
Zijn ammoniumsulfaat en aluminium hetzelfde?
 Timber Wolf-aanpassingen
Timber Wolf-aanpassingen  Waarom overstromingen nog steeds zo moeilijk te voorspellen en voor te bereiden zijn
Waarom overstromingen nog steeds zo moeilijk te voorspellen en voor te bereiden zijn Hoe schakelen gewas-veeteeltsystemen over op groene landbouwontwikkeling in het Baiyangdian Basin?
Hoe schakelen gewas-veeteeltsystemen over op groene landbouwontwikkeling in het Baiyangdian Basin?  Groene daken verbeteren de stedelijke omgeving - dus waarom hebben niet alle gebouwen ze?
Groene daken verbeteren de stedelijke omgeving - dus waarom hebben niet alle gebouwen ze? Waarom meer mensen dan ooit alleen wonen en wat dit betekent voor het milieu
Waarom meer mensen dan ooit alleen wonen en wat dit betekent voor het milieu
Hoofdlijnen
- Wie heeft echt DNA ontdekt?
- Wat is de studie van alle levensvormen?
- Welke van de volgende organellen is verantwoordelijk voor het afbreken van afval in cel?
- Het principe van individuele verschillen stelt dat de snelheids- en magnitude -aanpassingen aan training worden beperkt door uw verschillende genetica?
- Sardines nemen ons mee naar de bronnen van biodiversiteit in de Amazone-rivier
- Wat zijn interleukines?
- De wetenschappelijke methode kan het beste worden omschreven als een plan of set van.
- Onderzoek toont aan hoe genactie kan leiden tot diabetespreventie en -genezing
- Kunnen insecten dik worden?
- Bij longitudinaal onderzoek gedroogde bloedvlekmonsters spelen een rol
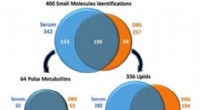
- Grafeen mapping 50 keer sneller

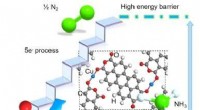
- Een nieuwe strategie voor de elektrochemische reductie van nitraat tot ammoniak
- Onderzoekers creëren eerste draagbare technologie voor het detecteren van cyanotoxinen in water

- Compact glasvezelapparaat werpt licht op ademanalyse in realtime

 Om moedig te gaan:Star Treks Shatner ruimtegebonden met Blue Origin
Om moedig te gaan:Star Treks Shatner ruimtegebonden met Blue Origin Studies bieden aanwijzingen over hoe alcoholisch gedrag wordt 'aangezet'
Studies bieden aanwijzingen over hoe alcoholisch gedrag wordt 'aangezet'  Welk percentage van een plantencel is water?
Welk percentage van een plantencel is water?  De acht meest overvloedige elementen in de aarde Crust
De acht meest overvloedige elementen in de aarde Crust Recente trends tonen het effect van de recessie op de Amerikaanse export van geavanceerde technologie
Recente trends tonen het effect van de recessie op de Amerikaanse export van geavanceerde technologie  Studie weerlegt het verhaal dat daklozen op straat servicebestendig zijn
Studie weerlegt het verhaal dat daklozen op straat servicebestendig zijn Wanneer je een bepaalde afstand in de richting schuift, hoe heet dat dan?
Wanneer je een bepaalde afstand in de richting schuift, hoe heet dat dan?  Onderzoeker onderzoekt hoe we de wereldwijde voedselvoorziening veerkrachtiger kunnen maken
Onderzoeker onderzoekt hoe we de wereldwijde voedselvoorziening veerkrachtiger kunnen maken
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

