
Wetenschap
Hoe zijn het smeltpunten en het kookpunt van moleculaire verbindingen verschillend van ionische verbindingen?
moleculaire verbindingen
* Lagere smelt- en kookpunten: Moleculaire verbindingen hebben over het algemeen veel lagere smelt- en kookpunten dan ionische verbindingen.
* Zwakke intermoleculaire krachten: De krachten die moleculen bij elkaar houden, zijn relatief zwak. Deze krachten worden intermoleculaire krachten genoemd (zoals van der Waals-krachten, waterstofbinding of dipool-dipool interacties). Er is minder energie nodig om deze krachten te overwinnen en de moleculen uit elkaar te breken.
* Covalente bindingen: Moleculaire verbindingen worden bij elkaar gehouden door covalente bindingen, waar atomen elektronen delen. Deze bindingen zijn sterk binnen het molecuul zelf, maar de aantrekkingskracht tussen moleculen zijn zwakker.
ionische verbindingen
* Hogere smelt- en kookpunten: Ionische verbindingen hebben veel hogere smelt- en kookpunten. Dit komt door de sterke elektrostatische krachten die de ionen bij elkaar houden in een kristalrooster.
* Sterke elektrostatische krachten: De tegengesteld geladen ionen in een ionische verbinding trekken elkaar sterk aan. Er is een aanzienlijke hoeveelheid energie voor nodig om deze sterke krachten te overwinnen en de ionen te scheiden.
* ionische bindingen: Ionische verbindingen vormen zich wanneer atomen elektronen overbrengen, waardoor positieve en negatief geladen ionen ontstaan. Deze ionen zijn gerangschikt in een zeer geordende, driedimensionale roosterstructuur.
Hier is een eenvoudige analogie:
Stel je een stapel knikkers voor (moleculaire verbinding). De knikkers worden bij elkaar gehouden door zwakke krachten. Je kunt ze gemakkelijk scheiden met een beetje moeite (lage smelten en kookpunten).
Stel je nu een strak gepakte doos met magneten voor (ionische verbinding). De magneten worden tot elkaar aangetrokken met sterke krachten. Er is veel meer kracht voor nodig om ze te scheiden (hoge smelt- en kookpunten).
Uitzonderingen:
* Netwerkcovalente verbindingen: Sommige moleculaire verbindingen, zoals diamant en kwarts, hebben ongelooflijk hoge smeltpunten. Dit komt omdat ze sterke covalente bindingen hebben die zich uitstrekken in een continu netwerk gedurende de hele structuur.
* polariteit: Polaire moleculaire verbindingen met sterke waterstofbruggen (zoals water) kunnen hogere smelt- en kookpunten hebben in vergelijking met niet-polaire moleculen.
Key Takeaway:
De sterkte van de krachten die de deeltjes (moleculen of ionen) bij elkaar houden, dicteert de hoeveelheid energie die nodig is om hun toestand van materie te veranderen. Sterkere krachten (zoals ionische bindingen) betekenen hogere smelt- en kookpunten, terwijl zwakkere krachten (zoals intermoleculaire krachten) lagere smelt- en kookpunten betekenen.
 Riffen beschermen kwetsbare Caribische vissen tegen klimaatverandering
Riffen beschermen kwetsbare Caribische vissen tegen klimaatverandering Wat voor soort klimaat is een bos?
Wat voor soort klimaat is een bos?  Gecombineerde voedingsstoffen en opwarming verhogen de methaanemissies van meren enorm
Gecombineerde voedingsstoffen en opwarming verhogen de methaanemissies van meren enorm Effecten van de hoogte van de vogelvoeders
Effecten van de hoogte van de vogelvoeders Veranderend landschap betekent dat sommige Arctische vijvers mogelijk een belangrijke bron van koolstofemissies kunnen zijn
Veranderend landschap betekent dat sommige Arctische vijvers mogelijk een belangrijke bron van koolstofemissies kunnen zijn
Hoofdlijnen
- Twee wetenschappers bestuderen gegevens die zijn verzameld tijdens een experiment en trekken verschillende conclusies. Hoe zou de wetenschappelijke gemeenschap hun meningsverschil aanpakken?
- Wat is de cel die gassen in gaat en een blad achterlaat?
- Welke erfelijkheidsfactoren werden beschreven door Mendel?
- Methode om overvloed te schatten, trends in Noord-Atlantische walvissen bevestigen achteruitgang
- Wat is koesteren?
- Wat is een voorbeeld van een marien angiosperm?
- Hoe eiwitaggregatie plaatsvindt in cellen
- Wetenschappers onderzoeken hoe verschillende vloeibare organellen in cellen worden gecreëerd
- Samen sterker:hoe eiwitfilamenten op elkaar inwerken
- Voedingseiwit kan de scherpte en bitterheid van extra vierge olijfolie elimineren

- Nieuw synthetisch protocol om een 3D poreus organisch netwerk te vormen

- Nieuwe technologie voor het produceren van poreus aluminium

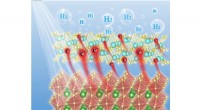
- Het maken van waterstof versnellen met een niet-edele metalen cokatalysator onder zichtbaar licht
- Bredere toepassingen voor de unboil an eiermachine

 Bodem herstellen om miljarden tonnen koolstof te absorberen:studie
Bodem herstellen om miljarden tonnen koolstof te absorberen:studie Nieuwe aanwijzingen voor de oorsprong van mysterieuze atmosferische golven op Antarctica
Nieuwe aanwijzingen voor de oorsprong van mysterieuze atmosferische golven op Antarctica EU zet stappen tegen chipmaker Broadcom in nieuwste Amerikaanse technische salvo
EU zet stappen tegen chipmaker Broadcom in nieuwste Amerikaanse technische salvo Review:2023 Toyota bZ4X vs. 2023 Volkswagen ID.4
Review:2023 Toyota bZ4X vs. 2023 Volkswagen ID.4 Wat is de moeilijkste fase in mitose om te herkennen?
Wat is de moeilijkste fase in mitose om te herkennen?  Mechanische nadelen van een hendelsysteem
Mechanische nadelen van een hendelsysteem Astronomen vinden kosmische gouden naald die al twee decennia begraven ligt
Astronomen vinden kosmische gouden naald die al twee decennia begraven ligt Hoe stel je de formule voor kwik-2-nitraat vast?
Hoe stel je de formule voor kwik-2-nitraat vast?
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

