
Wetenschap
Die elektronen die grotendeels verantwoordelijk zijn voor een chemisch gedrag van een atomen?
Dit is waarom:
* valentie -elektronen zijn de elektronen in het buitenste energieniveau van een atoom.
* Zij zijn degenen die interageren met andere atomen bij het vormen van chemische bindingen.
* Het aantal valentie -elektronen bepaalt de bindingscapaciteit van een atoom en de neiging om elektronen te winnen, verliezen of te delen.
* Dit dicteert op zijn beurt de soorten chemische verbindingen die een atoom kan vormen en de algehele reactiviteit ervan.
Bijvoorbeeld:
* natrium (na) Heeft één valentie -elektron, waardoor het zeer reactief is en dat elektron verliest om een positief ion te vormen.
* chloor (Cl) heeft zeven valentie -elektronen, waardoor het enthousiast is om één elektron te krijgen om zijn buitenste schaal te voltooien en een negatief ion te vormen.
* De interactie tussen natrium en chloor resulteert in de vorming van natriumchloride (NaCl), een stabiele verbinding met ionische bindingen.
 Een aardverschuiving dwong mij mijn huis te verlaten – en ik ervoer met eigen ogen dat wij er niet in slaagden om te gaan met de klimaatverandering
Een aardverschuiving dwong mij mijn huis te verlaten – en ik ervoer met eigen ogen dat wij er niet in slaagden om te gaan met de klimaatverandering  Video:Stillsuits voor steden verkennen
Video:Stillsuits voor steden verkennen Atmosferische turbulentie kan de vorming van wolkendruppels bevorderen
Atmosferische turbulentie kan de vorming van wolkendruppels bevorderen Het verband tussen stikstofbenutting en grondwaterkwaliteit is duidelijk
Het verband tussen stikstofbenutting en grondwaterkwaliteit is duidelijk Voorspelling van economische en demografische verschuivingen in de VS met een hogere resolutie
Voorspelling van economische en demografische verschuivingen in de VS met een hogere resolutie
Hoofdlijnen
- Wat is de belangrijkste functie in het wetenschappelijke proces?
- UA maakt deel uit van een groep die ontrafelt hoe de hersenen het geheugen beheren
- Wat zijn de vijf verschillende bewijslijnen voor evolutie?
- Wat is het hoofdmolecuul in een cel?
- Wat zijn de spoelen van DNA in de kern?
- Doet dierlijke cellen in het algemeen een celwand om de cel om te sluiten?
- Er is vlees gemaakt van cellen, en niet van vee. Maar zal het ooit het traditionele vlees vervangen?
- Studie suggereert dat nederige minnow de hitte aankan
- Wat zou Facebook te verbergen hebben?
- Zijderupsen zorgen voor een nieuwe draai aan kleverige moleculen

- Dubbel gedoteerde koolstofmicrosferen met sterk stikstof en zwavel voor supercondensatoren
- Onderzoekers ontwikkelen synthetische T-cellen die de vorm nabootsen, functie van menselijke versie

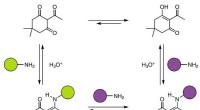
- Chemici maken thermohardend polymeer met behulp van amine en triketon dat recyclebaar is
- Het gebruik van schaaldieren bij het genezen van wonden - de toekomst van de geneeskunde?

 Is fenylalanine een zuur of een base?
Is fenylalanine een zuur of een base?  NASA's nieuwe naam Swift Mission bespioneert een vertraging van een komeet
NASA's nieuwe naam Swift Mission bespioneert een vertraging van een komeet Wat eten paramecium?
Wat eten paramecium?  De Centrale Andes had de grootste vulkaanuitbarsting van de afgelopen 5000 jaar
De Centrale Andes had de grootste vulkaanuitbarsting van de afgelopen 5000 jaar Welk element vormt twee gasvormige oxiden?
Welk element vormt twee gasvormige oxiden?  Een hydrozoan die eigenlijk een kolonie van vier soorten speciale poliepen is, hangen van elkaar af om te overleven?
Een hydrozoan die eigenlijk een kolonie van vier soorten speciale poliepen is, hangen van elkaar af om te overleven?  Na 150 jaar, een doorbraak in het begrijpen van de omzetting van CO2 naar elektrobrandstoffen
Na 150 jaar, een doorbraak in het begrijpen van de omzetting van CO2 naar elektrobrandstoffen Door de opwarming van de aarde zullen ecosystemen meer methaan produceren dan eerst werd voorspeld
Door de opwarming van de aarde zullen ecosystemen meer methaan produceren dan eerst werd voorspeld
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

