
Wetenschap
Hoeveel elektronen verliezen transitioonmetalen?
* variabele oxidatietoestanden: Overgangsmetalen staan bekend om hun vermogen om meerdere oxidatietoestanden te hebben. Dit betekent dat ze verschillende aantallen elektronen kunnen verliezen, afhankelijk van de chemische omgeving waarin ze zich bevinden.
* D-orbitale betrokkenheid: Overgangsmetalen hebben gedeeltelijk gevulde D-orbitalen. Deze D-orbitalen zijn betrokken bij de binding en het aantal verloren elektronen kan de manier veranderen waarop het metaal interageert met andere elementen.
Voorbeelden:
* ijzer (Fe): Kan oxidatietoestanden hebben van +2 (2 elektronen verliezen) of +3 (3 elektronen verliezen).
* koper (cu): Kan oxidatietoestanden hebben van +1 (1 elektron verliezen) of +2 (2 elektronen verliezen).
* Mangaan (Mn): Kan oxidatietoestanden hebben variërend van +2 tot +7.
factoren die van invloed zijn op elektronenverlies:
* De identiteit van het metaal: Verschillende metalen hebben verschillende neigingen om elektronen te verliezen.
* De aard van de liganden: De moleculen of ionen rond het metaalatoom kunnen de oxidatietoestand ervan beïnvloeden.
* De reactieomstandigheden: Factoren zoals temperatuur en druk kunnen het aantal verloren elektronen beïnvloeden.
Samenvattend hebben overgangsmetalen geen vast aantal elektronen dat ze verliezen. Het aantal verloren elektronen hangt af van het specifieke metaal, de chemische omgeving en de reactieomstandigheden.
 Welke belangrijke molecule van erfelijkheid bevat fosfor?
Welke belangrijke molecule van erfelijkheid bevat fosfor?  Wetenschappers vinden nieuwe manieren om chemicaliën voor bioraffinage te gebruiken
Wetenschappers vinden nieuwe manieren om chemicaliën voor bioraffinage te gebruiken Wat is de normaliteit van 0,1 N acetaat?
Wat is de normaliteit van 0,1 N acetaat?  Rock Salt Vs. Tafelzout tot smeltijs
Rock Salt Vs. Tafelzout tot smeltijs  Wat gebeurt er wanneer de testbuis die groen pigment bevat, in kokend water wordt geplaatst?
Wat gebeurt er wanneer de testbuis die groen pigment bevat, in kokend water wordt geplaatst?
 Vervuilde lucht in Delhi, vergelijkbaar met de doodstraf, zeg dokters
Vervuilde lucht in Delhi, vergelijkbaar met de doodstraf, zeg dokters Is uil carnivore of herbivoor?
Is uil carnivore of herbivoor?  EU-klimaatleiderschap in twijfel omdat blok het doel voor 2030 gaat missen
EU-klimaatleiderschap in twijfel omdat blok het doel voor 2030 gaat missen Een ongemakkelijke waarheid over een ongemakkelijke waarheid
Een ongemakkelijke waarheid over een ongemakkelijke waarheid Vrijdagessay:waarom volwassenen nog steeds sprookjes nodig hebben
Vrijdagessay:waarom volwassenen nog steeds sprookjes nodig hebben
Hoofdlijnen
- Wat is een zelfoverdraagbaar plasmide?
- Naar welk orgelsysteem behoort het ileum?
- Betekent het woord mijten hetzelfde als mitose?
- Chinese fruitvlieggenomen onthullen mondiale migraties en herhaalde evolutie
- Wat betekent de aanwezigheid van Rh-antigeen?
- Waar zou je een cel vinden die een groot aantal chloroplasten bevatte?
- Wat maakt altijd deel uit van de wetenschappelijke methode gecontroleerde experimenten of gegevensverzameling?
- Is een schimmel een voorbeeld van nuttig organisme?
- Relaties tussen mitose in eukaryote cellen en binaire fissie in Prokaryoten
- Onderzoek toont aan dat het doen van de twist hot is, ontspannen is cool

- Een nieuwe methode voor proximity-labeling op nanometerschaal die zich richt op histidine-residuen

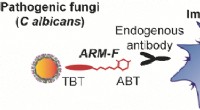
- Neutralisatie van pathogene schimmels met immunotherapeutica met kleine moleculen
- Wetenschappers bij ESS, Zweeds wateronderzoek, ORNL gebruikt VISION om te kijken naar veelvoorkomende verontreinigingen voor toepassingen in schoner water

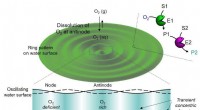
- Regeling in de tijd van chemische reacties met alleen hoorbaar geluid
 Is 'dieseltop' de laatste kans voor de favoriete motor van Duitsland?
Is 'dieseltop' de laatste kans voor de favoriete motor van Duitsland?  Vlinders inspireren tot de creatie van de lichtste verf ter wereld
Vlinders inspireren tot de creatie van de lichtste verf ter wereld  Wat is de oorsprong en betekenis van naam?
Wat is de oorsprong en betekenis van naam?  $60 miljoen om het Great Barrier Reef te redden is een druppel op een gloeiende plaat, maar we moeten het proberen
$60 miljoen om het Great Barrier Reef te redden is een druppel op een gloeiende plaat, maar we moeten het proberen Akoestische monitoring geeft een holistisch beeld van de biodiversiteit
Akoestische monitoring geeft een holistisch beeld van de biodiversiteit Hoeveel 750 ml in ounces?
Hoeveel 750 ml in ounces?  Onderzoekers verbeteren efficiëntie van goedkope zonnecellen
Onderzoekers verbeteren efficiëntie van goedkope zonnecellen Koolzuur in frisdranken meten voor een wetenschappelijk project
Koolzuur in frisdranken meten voor een wetenschappelijk project
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

