
Wetenschap
Wat zijn sterke en zwakke moleculaire krachten?
Strong versus zwakke moleculaire krachten
moleculaire krachten zijn de aantrekkelijke of afstotende krachten die tussen moleculen bestaan. Deze krachten bepalen veel fysieke eigenschappen van stoffen, zoals smeltpunt, kookpunt en oplosbaarheid.
Hier is een uitsplitsing van sterke en zwakke moleculaire krachten:
Sterke moleculaire krachten:
* Covalente bindingen: Dit zijn het sterkste type moleculaire kracht, waarbij elektronen tussen atomen worden gedeeld. Ze houden atomen bij elkaar in een molecuul. Voorbeelden zijn de bindingen in water (H₂o) en methaan (CH₄).
* ionische bindingen: Deze omvatten de elektrostatische aantrekkingskracht tussen tegengesteld geladen ionen. Ze zijn ook sterk maar zwakker dan covalente bindingen. Een voorbeeld is de binding in natriumchloride (NaCl).
Zwakke moleculaire krachten:
* van der Waals krachten: Dit zijn zwakke, korte-afstandskrachten die voortvloeien uit tijdelijke schommelingen in elektronenverdeling rond moleculen. Ze zijn verder verdeeld in:
* Dispersietroepen in Londen: Voorkomen in alle moleculen en zijn zelfs aanwezig in edelgassen. Ze zijn zwakker dan dipool-dipoolkrachten.
* Dipole-Dipole Forces: Komen op tussen polaire moleculen, waarbij het positieve uiteinde van het ene molecuul wordt aangetrokken door het negatieve uiteinde van het andere.
* waterstofbinding: Een speciaal type dipool-dipoolinteractie die optreedt wanneer een waterstofatoom wordt gebonden aan een zeer elektronegatief atoom (zoals zuurstof, stikstof of fluor). Dit is een relatief sterk type van der Waals -kracht.
Belangrijkste verschillen:
| Feature | Sterke moleculaire krachten | Zwakke moleculaire krachten |
| ----------------- | ----------------------- | -------------------------- |
| Binding Sterkte | Sterk | Zwak |
| Interactietype | Binnen moleculen | Tussen moleculen |
| Voorbeelden | Covalent, Ionic | Van der Waals |
| Effect op eigenschappen | Hogere smelt-/kookpunten, lagere dampdruk | Lagere smelt-/kookpunten, hogere dampdruk |
Samenvattend:
* Sterke moleculaire krachten Houd atomen bij elkaar in een molecuul en vereisen aanzienlijke energie om te breken.
* Zwakke moleculaire krachten zijn verantwoordelijk voor de interacties tussen moleculen en kunnen eigenschappen beïnvloeden zoals kookpunt en oplosbaarheid.
Het begrijpen van de sterkte van moleculaire krachten is cruciaal voor het voorspellen en verklaren van het gedrag van verschillende stoffen.
 Het mosgenoom laat zien hoe planten het land binnendrongen en leerden hittedroogte te overleven
Het mosgenoom laat zien hoe planten het land binnendrongen en leerden hittedroogte te overleven  Duitsers zijn voorstander van een snelle stopzetting van het gebruik van steenkool naarmate het besluit nadert
Duitsers zijn voorstander van een snelle stopzetting van het gebruik van steenkool naarmate het besluit nadert Gezondheidscrisis:jaarlijks kan tot een miljard ton afval in de open lucht worden verbrand
Gezondheidscrisis:jaarlijks kan tot een miljard ton afval in de open lucht worden verbrand We kunnen luchthavens niet uitbreiden nadat we een klimaatnoodtoestand hebben uitgeroepen - laten we in plaats daarvan overschakelen op koolstofarm transport
We kunnen luchthavens niet uitbreiden nadat we een klimaatnoodtoestand hebben uitgeroepen - laten we in plaats daarvan overschakelen op koolstofarm transport Hoe hevige herfst- en winterwinden de branden in Californië voeden
Hoe hevige herfst- en winterwinden de branden in Californië voeden
Hoofdlijnen
- Organismen in een ecosysteem zijn verbonden met elkaar verbonden door?
- Wat betekent nakomelingen?
- griezelige vraag bij vogelgriep:hoe dood je miljoenen pluimvee
- Een klokvormige kromme van fenotypische variatie is een weergave van?
- Waarom kan een enkel cellen organisme zoals Paramecium buiten het lichaam overleven terwijl de menselijke cel zou sterven?
- Hoe Hydra-dieren hun eigen hoofd regenereren
- Wat is een adaptief voordeel voor het beperken van DNA in een kern?
- Nieuw onderzoek vergroot het inzicht in wat het menselijke darmmicrobioom vormt
- Welke vissen migreren?
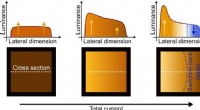
- Hete OLED's kunnen terugschakelen
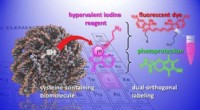
- Nieuwe chemische hulpmiddelen om biomoleculen te wijzigen en te bestuderen
- Doorbraak kunstmatige fotosynthese komt dichterbij

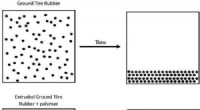
- Polymeren effenen de weg voor een breder gebruik van gerecyclede banden in asfalt
- Ontdekking kan leiden tot nieuw katalysatorontwerp om stikstofoxiden in dieseluitlaatgassen te verminderen

 NASA's Curiosity-rover wil zijn ritme terugkrijgen
NASA's Curiosity-rover wil zijn ritme terugkrijgen NASA-afbeelding legt de aarde vast tussen de ringen van Saturnus
NASA-afbeelding legt de aarde vast tussen de ringen van Saturnus Poreuze kristallen gebruiken om licht te oogsten
Poreuze kristallen gebruiken om licht te oogsten Het groeperen van studenten in op vaardigheden gebaseerde sets houdt minder bekwame leerlingen tegen
Het groeperen van studenten in op vaardigheden gebaseerde sets houdt minder bekwame leerlingen tegen Hoe worden vulkanenuitbarstingen gemeten?
Hoe worden vulkanenuitbarstingen gemeten?  NASA's Terra-satelliet analyseert Caribische tropische depressie 14
NASA's Terra-satelliet analyseert Caribische tropische depressie 14 Je telefoon opladen via een openbare USB-poort? Pas op voor sappersen
Je telefoon opladen via een openbare USB-poort? Pas op voor sappersen Wetenschappers klauteren om lading te bouwen voor maanlanding in 2021
Wetenschappers klauteren om lading te bouwen voor maanlanding in 2021
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

