
Wetenschap
Welke van deze stoffen heeft het laagste kookpunt KCL CO2CH2O?
* KCL (kaliumchloride): Dit is een ionische verbinding. Ionische verbindingen hebben zeer sterke elektrostatische attracties tussen hun ionen, wat leidt tot hoge smelt- en kookpunten.
* CO2 (koolstofdioxide): Dit is een niet -polair molecuul. Niet -polaire moleculen hebben zwakke dispersiekrachten in Londen, die de enige aanwezige intermoleculaire krachten zijn. Dit resulteert in relatief lage kookpunten.
* CH2O (formaldehyde): Dit is een polair molecuul. Polaire moleculen hebben dipool-dipoolinteracties naast de dispersiekrachten in Londen. Dipool-dipoolinteracties zijn sterker dan dispersiekrachten in Londen, maar nog steeds zwakker dan ionische bindingen.
Daarom heeft CO2 (koolstofdioxide) het laagste kookpunt.
Dit is waarom:
* Zwakste intermoleculaire krachten: CO2 heeft alleen zwakke dispersiekrachten in Londen tussen zijn moleculen.
* Kleinere moleculaire grootte: CO2 is een klein molecuul, dat de sterkte van deze krachten verder vermindert.
 Feiten over de Wisconsin State Bird - Amerikaanse Robin
Feiten over de Wisconsin State Bird - Amerikaanse Robin India begint aardverschuiving, opruimen van overstromingen terwijl dodelijke moessonregens afnemen
India begint aardverschuiving, opruimen van overstromingen terwijl dodelijke moessonregens afnemen Binnentemperatuur van de aarde nemen:verrassende nieuwe studie vindt dat de mantel heter is dan we dachten
Binnentemperatuur van de aarde nemen:verrassende nieuwe studie vindt dat de mantel heter is dan we dachten Een blik op hoe het veranderende klimaat de gebouwenvoorraad in de staat New York beïnvloedt
Een blik op hoe het veranderende klimaat de gebouwenvoorraad in de staat New York beïnvloedt Lake Maracaibo:vervuild door een permanent eb en vloed
Lake Maracaibo:vervuild door een permanent eb en vloed
Hoofdlijnen
- Waarom wetenschappers een ondergronds mysterie willen oplossen over waar microben leven
- Hoe Beschrijf de drie stappen in mendelstudies van erwtenplanten?
- Onderzoek toont het potentieel aan van zuidelijke lisdodde voor fytoremediatie van gebieden die zijn verontreinigd met mijnafval
- Genetische drift, en niet natuurlijke selectie, geïdentificeerd als de belangrijkste factor die soortvorming bij bedreigde soorten pupfish aanstuurt
- Onderzoek bepaalt of culturen games spelen die overeenkomen met hoe coöperatief ze zijn
- Studie van keverflagellum biedt mogelijke manier om medische hulpmiddelen te verbeteren
- Welke stap in de wetenschappelijke methode maakt u conclusies?
- Bijenvival:herstelt de bijenpopulatie in Texas zich?
- Welke aanpassingen hebben ghaf-bomen?
- Het membraan in membraanloze organellen begrijpen
- Smartphone-testplekken vergiftigd waterrisico voor miljoenen levens

- Materiaalwetenschappers ontdekken ontwerpgeheimen van bijna onverwoestbaar insect

- De eeuwigheid modelleren in het rotslaboratorium

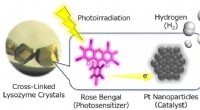
- Wetenschappers gebruiken eiwitten voor de productie van schone energie
 Waarom is het type binding tussen zuurstof en silicium schadelijk voor het milieu?
Waarom is het type binding tussen zuurstof en silicium schadelijk voor het milieu?  Welk volume bezet 1 mol gasdeeltjes bij RTP?
Welk volume bezet 1 mol gasdeeltjes bij RTP?  Huisrepublikeinen twijfelen aan telecom over locatietracking
Huisrepublikeinen twijfelen aan telecom over locatietracking Is ijzer een pure substantie of mengsel?
Is ijzer een pure substantie of mengsel?  Overeenkomsten tussen huidcellen en zenuwen
Overeenkomsten tussen huidcellen en zenuwen  Wie was de eerste persoon die ziektekiemen ontdekte?
Wie was de eerste persoon die ziektekiemen ontdekte?  Siliciumchip met geïntegreerde laser:licht van een nanodraad
Siliciumchip met geïntegreerde laser:licht van een nanodraad Doorbreken van de absorptielimiet van silicium in de richting van het korte-golflengte-infraroodgolflengtebereik via spanningstechniek
Doorbreken van de absorptielimiet van silicium in de richting van het korte-golflengte-infraroodgolflengtebereik via spanningstechniek
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

