
Wetenschap
Wat is een pH van zwakke alkali?
Dit is waarom:
* pH -schaal: De pH -schaal meet de zuurgraad of alkaliteit van een oplossing. Het varieert van 0 tot 14.
* zuren: Zuren hebben een pH minder dan 7.
* neutraal: Een neutrale oplossing heeft een pH van 7.
* alkalis (bases): Alkalis of bases hebben een pH groter dan 7.
zwakke alkalisten zijn degenen die slechts gedeeltelijk ioniseren in oplossing, wat betekent dat ze niet al hun hydroxide-ionen (OH-) in de oplossing vrijgeven. Dit resulteert in een lagere concentratie OH- vergeleken met sterke alkalisten, wat leidt tot een pH dichter bij 7.
Voorbeelden van zwakke alkalis:
* Ammoniak (NH3)
* Natriumbicarbonaat (NAHCO3)
* Magnesiumhydroxide (Mg (OH) 2)
Belangrijke opmerking: De exacte pH van een zwakke alkali zal afhangen van de concentratie en de specifieke verbinding.
 Onderzoekers ontwikkelen potentieel goedkope, emissiearme technologie die methaan kan omzetten zonder CO2 . te vormen
Onderzoekers ontwikkelen potentieel goedkope, emissiearme technologie die methaan kan omzetten zonder CO2 . te vormen De leiding nemen om de juiste balans te vinden voor geavanceerde opto-elektronische apparaten
De leiding nemen om de juiste balans te vinden voor geavanceerde opto-elektronische apparaten Wat is een stof die niet in eenvoudiger kan worden opgesplitst met alle kenmerken van inhoud?
Wat is een stof die niet in eenvoudiger kan worden opgesplitst met alle kenmerken van inhoud?  Wat is de exacte reactie tussen natriummetabisulfiet en broom?
Wat is de exacte reactie tussen natriummetabisulfiet en broom?  Welke stof verandert de kleur van pH -papier in groenachtig?
Welke stof verandert de kleur van pH -papier in groenachtig?
 Eco-activistische aanvallen op museumkunstwerken vragen ons om erachter te komen wat we waarderen
Eco-activistische aanvallen op museumkunstwerken vragen ons om erachter te komen wat we waarderen  Zou het dierenleven op aarde mogelijk zijn zonder planten?
Zou het dierenleven op aarde mogelijk zijn zonder planten?  Grootte is belangrijk bij luchtvervuiling, maar het is niet genoeg
Grootte is belangrijk bij luchtvervuiling, maar het is niet genoeg Het verband tussen fracking en aardbevingen begrijpen
Het verband tussen fracking en aardbevingen begrijpen Herwild 25% van het VK voor minder klimaatverandering, meer dieren in het wild en een leven dichter bij de natuur
Herwild 25% van het VK voor minder klimaatverandering, meer dieren in het wild en een leven dichter bij de natuur
Hoofdlijnen
- Fun Biology Presentatie Onderwerpen
- Wat is de functie van NAD bij de glycolyse?
- Hoe zijn wetenschapstechnologie en samenleving allemaal gerelateerd?
- Zou een DNA meer op de krab of die limpet lijken?
- Het menselijk lichaam bestaat meestal uit wat?
- Wat is de samenstelling van Luria Agar?
- Hoe bepaalt een bioloog of iets levend of niet-levend is?
- Wat is de vorm van een levercel voor dieren en waarom?
- Apen vertonen dramatisch verschillende vroege immuunreacties vergeleken met apen
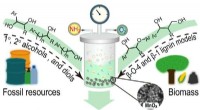
- Nieuwe strategie maakt opeenvolgende splitsing en functionalisering van C–C-bindingen in alcoholen mogelijk
- Water, overal water - en het is vreemder dan je denkt

- Hoe chloor next-gen zonnecellen stabiliseert op atomaire schaal

- C. elegans rondwormen oogsten een essentieel co-enzym uit de bacteriën die ze consumeren

- Modellering van biomimetische collageen-ligand-interacties om intrafibrillaire mineralisatie te begrijpen
 Geen vertroebelde oordelen:geostationaire satelliet een alternatief voor het monitoren van landoppervlakken
Geen vertroebelde oordelen:geostationaire satelliet een alternatief voor het monitoren van landoppervlakken Drone-foto's bieden snellere, goedkopere gegevens over de belangrijkste Antarctische soorten
Drone-foto's bieden snellere, goedkopere gegevens over de belangrijkste Antarctische soorten Een wegwerpbare levende laser geprint op chip voor drugsscreening
Een wegwerpbare levende laser geprint op chip voor drugsscreening Wetenschappers ontdekken hoe sommige bacteriën ijzer van hun menselijke gastheren kunnen stelen
Wetenschappers ontdekken hoe sommige bacteriën ijzer van hun menselijke gastheren kunnen stelen  Heks hiervan is geen monatomisch element F Kr Rn Ne?
Heks hiervan is geen monatomisch element F Kr Rn Ne?  Nieuwe theorie toont eigenaardige Janus-interface een gemeenschappelijk mechanisme in de groei van koolstofnanobuisjes
Nieuwe theorie toont eigenaardige Janus-interface een gemeenschappelijk mechanisme in de groei van koolstofnanobuisjes Homoseksuele mannen die homoseksueel klinken, ondervinden meer stigma en discriminatie van heteroseksuele leeftijdsgenoten
Homoseksuele mannen die homoseksueel klinken, ondervinden meer stigma en discriminatie van heteroseksuele leeftijdsgenoten Studie onthult mechanismen die ijsvorming bevorderen die verantwoordelijk zijn voor stroomonderbrekingen
Studie onthult mechanismen die ijsvorming bevorderen die verantwoordelijk zijn voor stroomonderbrekingen
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

