
Wetenschap
Hoe zal de dampdruk van zuiver water zich verhouden tot een waterige oplossing natriumchloride?
* dampdruk is de druk die wordt uitgeoefend door de damp van een vloeistof in evenwicht met zijn vloeibare fase.
* colligatieve eigenschappen zijn eigenschappen van oplossingen die afhankelijk zijn van de concentratie van opgeloste deeltjes, niet op hun identiteit. Het verlagen van dampdruk is een van deze colligatieve eigenschappen.
* natriumchloride (NaCl) is een ionische verbinding die dissocieert in twee ionen (Na+ en Cl-) wanneer opgelost in water. Dit betekent dat een 1 m oplossing van NaCl een hogere concentratie van opgeloste deeltjes zal hebben dan een oplossing van 1 m van een niet-ionische verbinding zoals suiker.
Hoe het werkt:
* Puur water: Watermoleculen hebben een relatief hoge neiging om te ontsnappen in de dampfase, wat leidt tot een hogere dampdruk.
* waterige NaCl -oplossing: De opgeloste ionen (Na+ en Cl-) interageren met de watermoleculen, waardoor het moeilijker is voor watermoleculen om te ontsnappen in de dampfase. Dit vermindert de dampdruk.
Samenvattend: De aanwezigheid van opgeloste natriumchloride -ionen in de oplossing verlaagt de dampdruk in vergelijking met zuiver water. Dit is een direct gevolg van de colligatieve eigenschap die bekend staat als dampdrukverlaging.
 Wat is de relatie tussen smeltpunt van een olie en hoe onverzadigd deze is?
Wat is de relatie tussen smeltpunt van een olie en hoe onverzadigd deze is?  Kleurstoffen uit atmosferische kooldioxide
Kleurstoffen uit atmosferische kooldioxide Wat is de kleur van kristallen benzimidazol?
Wat is de kleur van kristallen benzimidazol?  Is de volgende vergelijking gebalanceerd CS2 plus 2Cl2 CCl4 S2Cl2?
Is de volgende vergelijking gebalanceerd CS2 plus 2Cl2 CCl4 S2Cl2?  Is het oplossen van jodium in alcohol een chemische of fysische verandering?
Is het oplossen van jodium in alcohol een chemische of fysische verandering?
 Bescherm oceaan tegen onomkeerbare veranderingen:experts roepen op tot acht dringende maatregelen
Bescherm oceaan tegen onomkeerbare veranderingen:experts roepen op tot acht dringende maatregelen Hoe de Tibetaanse verheffing de evolutie van de westelijke circulatie beïnvloedt
Hoe de Tibetaanse verheffing de evolutie van de westelijke circulatie beïnvloedt Een nieuw algoritme verbetert de vliegveiligheid en vermindert vertragingen
Een nieuw algoritme verbetert de vliegveiligheid en vermindert vertragingen De wind in Californië neemt af, maar het brandgevaar blijft groot
De wind in Californië neemt af, maar het brandgevaar blijft groot In het Canadese Quebec waren de bewoners nijdig over de opkomst van de mijnbouw
In het Canadese Quebec waren de bewoners nijdig over de opkomst van de mijnbouw
Hoofdlijnen
- Er zit een diepere vis in de zee
- Wat is het verschil tussen een Centriole en een Centrosome?
- Wat is de wetenschappelijke naam Ladybird?
- Is borstkanker een sekschromosoom?
- Wat is de functie van een rattenmilt?
- Wat is anti-biologie?
- Wat zijn ovacytes?
- In 1910 ontdekte Thomas Morgan een bepaald overervingspatroon in fruitvliegen die bekend staan als seksverbinding.
- Wat zijn de twee delen van het skeletstelsel?
- Nieuwe technologie kan goedkopere, sneller voedsel testen

- Onderzoekers onderzoeken hersenziekte-veroorzakende eiwitten op atomair niveau
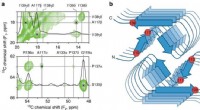
- Wetenschappers kapen bacteriën om de productie van medicijnen te vergemakkelijken
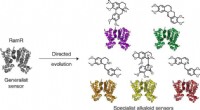
- Onderzoekers ontdekken proces om psilocybine duurzaam te produceren een kandidaat-geneesmiddel dat kan helpen bij de behandeling van depressie

- Chemici maken een molecuul dat kan helpen bij de behandeling van hartaandoeningen en het opsporen van virussen
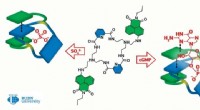
 Welke soorten chemicaliën zullen de werking van een enzym versnellen?
Welke soorten chemicaliën zullen de werking van een enzym versnellen?  Wat is de enige stralingsenergie die je kunt zien?
Wat is de enige stralingsenergie die je kunt zien?  Wat is een Stryker-voertuig?
Wat is een Stryker-voertuig?  Open-source software stelt onderzoekers in staat structuren op nanoschaal in realtime te visualiseren
Open-source software stelt onderzoekers in staat structuren op nanoschaal in realtime te visualiseren Hoe identificeer je Raw Gold
Hoe identificeer je Raw Gold Het mysterie van de grotgarnalen oplossen:geologie en evolutie in actie
Het mysterie van de grotgarnalen oplossen:geologie en evolutie in actie Wat is de chemische vergelijking kalium en lood nitraat om lood te vormen?
Wat is de chemische vergelijking kalium en lood nitraat om lood te vormen?  Scheidingen tussen aardbevingen onthullen duidelijke patronen
Scheidingen tussen aardbevingen onthullen duidelijke patronen
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

