
Wetenschap
Is ijzerfosfaat oplosbaar in water?
IJzerfosfaat (FEPO₄) is onoplosbaar in water.
Dit is waarom:
* Regels voor oplosbaarheid: Over het algemeen zijn fosfaten (PO₄³⁻) onoplosbaar in water, behalve die met groep 1 kationen (zoals Na⁺, K⁺) en ammonium (NH₄⁺).
* ionische verbindingen: IJzerfosfaat is een ionische verbinding, wat betekent dat het wordt gevormd door de elektrostatische aantrekkingskracht tussen ijzer (Fe³⁺) en fosfaat (po₄³⁻) ionen. De sterke aantrekkingskracht tussen deze ionen maakt het moeilijk voor hen om in water te dissociëren.
Daarom zal ijzerfosfaat niet significant oplossen in water.
 Studie:gletsjers in Azië worden geconfronteerd met enorme smelting door de opwarming van de aarde
Studie:gletsjers in Azië worden geconfronteerd met enorme smelting door de opwarming van de aarde Video:Hoe zullen kuststeden zich aanpassen aan de zeespiegelstijging?
Video:Hoe zullen kuststeden zich aanpassen aan de zeespiegelstijging? Feiten over nijlpaarden
Feiten over nijlpaarden  Nieuw onderzoek laat zien hoe hekken trekvogels in het Westen hinderen
Nieuw onderzoek laat zien hoe hekken trekvogels in het Westen hinderen  Mode-industrie haalt groene doelstellingen niet:rapport
Mode-industrie haalt groene doelstellingen niet:rapport
Hoofdlijnen
- Waar zijn plantes van gemaakt?
- Wat eten sprinkhanen? Het is niet alleen gras! Onderzoek toont overeenkomsten met zoogdiertanden als nooit tevoren
- De ontdekking van cellen is het meest direct gekoppeld van de ontwikkeling de?
- Hoeveel chromosomen heeft een spinwortelplant?
- Het ontrafelen van de metabolische mysteries van grasmatten onder hittestress
- Dr. YouTube... wat is uw diagnose?
- Het benutten van broodvruchtzetmeel voor de productie van bio-ethanol
- Honden huilen meer als ze herenigd worden met hun baasjes
- Onderzoek toont aan hoe een gen planten helpt hun eiwitproductie in stressvolle tijden te beheersen
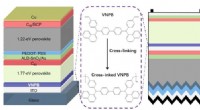
- Verknoopte gatentransportlagen voor hoogrenderende perovskiet-tandemzonnecellen
- Polymere membranen gebruiken om industriële scheidingen op te ruimen

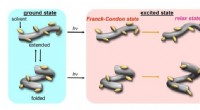
- Onder druk:eiwit-nabootsende moleculen manipuleren met hydrostatische druk
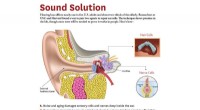
- Het verbinden van hoorhulpmoleculen met het oorbeen
- Raman-spectroscopie biedt een niet-invasieve manier om herprogrammering van cellen te volgen

 Wat zijn voorbeelden van gedissipeerde energie?
Wat zijn voorbeelden van gedissipeerde energie?  Wat is een unitellulair organinsman?
Wat is een unitellulair organinsman?  Orkanen Irma en Jose:wat we weten
Orkanen Irma en Jose:wat we weten  Hoeveel procent oleum is zwavelzuur?
Hoeveel procent oleum is zwavelzuur?  Kunnen slechte wiskundige vaardigheden uw risico op marktafscherming vergroten?
Kunnen slechte wiskundige vaardigheden uw risico op marktafscherming vergroten?  Is de massa van alle chlooratomen altijd 35,47?
Is de massa van alle chlooratomen altijd 35,47?  Nauwkeurige antitumorstrategie bereikt via fotoschakelbare met lanthanide gedoteerde nanodeeltjes
Nauwkeurige antitumorstrategie bereikt via fotoschakelbare met lanthanide gedoteerde nanodeeltjes LED Vs. CF-lampen
LED Vs. CF-lampen
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

