
Wetenschap
Wat is het gebruik van de atomen van verschillende elementen zodat ze zich op dezelfde manier gedragen?
* Elektronen bepalen chemisch gedrag: Elektronen zijn de deeltjes die betrokken zijn bij chemische binding. De manier waarop atomen met elkaar omgaan, hangt af van hun elektronenopstelling.
* valentie -elektronen zijn de sleutel: Valentie -elektronen zijn de buitenste elektronen in een atoom. Zij zijn degenen die het meest waarschijnlijk deelnemen aan chemische reacties.
* Vergelijkbare valentie -elektronenconfiguraties leiden tot vergelijkbaar gedrag: Elementen met hetzelfde aantal valentie -elektronen en een vergelijkbare opstelling van deze elektronen hebben de neiging vergelijkbare chemische bindingen te vormen en vertonen vergelijkbare chemische eigenschappen.
Bijvoorbeeld:
* Groep 1 (Alkali metalen): Alle alkali -metalen hebben één valentie -elektron. Dit geeft hen een sterke neiging om dat elektron te verliezen en een +1 lading te vormen, wat resulteert in een vergelijkbare reactiviteit.
* Groep 17 (halogenen): Alle halogenen hebben zeven valentie -elektronen. Ze hebben een sterke neiging om één elektron te krijgen om een stabiele octetconfiguratie te bereiken, wat ook tot vergelijkbare reactiviteit leidt.
Belangrijke opmerking: Hoewel valentie-elektronen een sleutelfactor zijn, zijn er andere aspecten van elektronenconfiguratie die chemisch gedrag kunnen beïnvloeden, zoals de aanwezigheid van lege D-orbitalen of het energieniveau van de valentieschil.
Samenvattend is de gelijkenis in chemisch gedrag tussen atomen van verschillende elementen vaak geworteld in de gelijkenis van hun valentie -elektronenconfiguraties, die hun vermogen regelt om chemische bindingen te vormen.
 Uitbarsting van Kilauea stimuleert creatie van realtime luchtvervuilingsnetwerk
Uitbarsting van Kilauea stimuleert creatie van realtime luchtvervuilingsnetwerk Historisch kasteel in het VK loopt gevaar door klimaatverandering:heritage body
Historisch kasteel in het VK loopt gevaar door klimaatverandering:heritage body NASA's GRACE:wat onderzoekers hebben geleerd van water in beweging
NASA's GRACE:wat onderzoekers hebben geleerd van water in beweging Veel vlees eten is slecht voor het milieu, maar we weten niet genoeg hoe de consumptie verandert
Veel vlees eten is slecht voor het milieu, maar we weten niet genoeg hoe de consumptie verandert  Wat zijn de verschillen tussen een huis en een menselijk lichaam?
Wat zijn de verschillen tussen een huis en een menselijk lichaam?
Hoofdlijnen
- Wat eten bruine kikkers?
- Welke psycholoog zei nog dat wat we bereiken te wijten is aan de samenstelling van onze genen?
- Wat is de functie van zaadwortel in dicot?
- Wat is een eigenschap waarmee een organisme beter kan overleven of zich beter voortplant dan anderen zonder de in specifieke omgeving?
- Europa's oudste boom groeit nog steeds
- Wat worden granulocyten?
- Wat wordt door de bloedbaan naar de huid gedragen?
- Geschiedenis van de aarde: tijdlijn, proces en feiten
- Wetenschappers ontdekken hoe immuuncellen voelen wie ze zijn
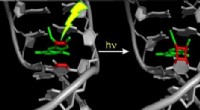
- Licht werpen op het reactiemechanisme van PUVA-lichttherapie voor huidziekten
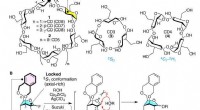
- Onderzoekers vinden een manier om kleine cyclodextrines te synthetiseren
- Bioactief boraatglas op nanoschaal:een materiaal van de volgende generatie voor huidgenezing

- Universele latente aniondonoren voor ultralage werkfunctie-oplossing-verwerkbare elektroden

- Een stap in de richting van metaal-organische raamwerksynthese
 Honderdtien liter stedelijk regenwater wordt elke seconde schoongemaakt
Honderdtien liter stedelijk regenwater wordt elke seconde schoongemaakt Wie was de man of vrouw waarnaar Chamberlin -gletsjer werd vernoemd?
Wie was de man of vrouw waarnaar Chamberlin -gletsjer werd vernoemd?  Waarom geven we het slachtoffer de schuld?
Waarom geven we het slachtoffer de schuld?  Kan deze vergelijking in evenwicht worden gebracht? Ammoniumfosfaat plus loodnitraat is gelijk aan nitraat?
Kan deze vergelijking in evenwicht worden gebracht? Ammoniumfosfaat plus loodnitraat is gelijk aan nitraat?  Nieuw raamwerk maakt AI-systemen transparanter zonder in te boeten aan prestaties
Nieuw raamwerk maakt AI-systemen transparanter zonder in te boeten aan prestaties Het magnetische schild van de aarde dreunt als een trommel wanneer het wordt geraakt door impulsen
Het magnetische schild van de aarde dreunt als een trommel wanneer het wordt geraakt door impulsen Dorian kruipt naar de Amerikaanse kust, verzwakking tot categorie 2 storm
Dorian kruipt naar de Amerikaanse kust, verzwakking tot categorie 2 storm Wat is de betekenis van emissiemeting bij het begrijpen van het gedrag van een bepaald astronomisch object?
Wat is de betekenis van emissiemeting bij het begrijpen van het gedrag van een bepaald astronomisch object?
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

