
Wetenschap
Heeft zout invloed op het smelten van ijs of niet?
* Het vriespunt verlagen: Zout verlaagt het vriespunt van water. Dit betekent dat een zoute wateroplossing kouder moet zijn dan zuiver water om te bevriezen.
* hoe het werkt: Wanneer zout wordt toegevoegd aan ijs, lost het op in de dunne laag water die zich natuurlijk op het oppervlak vormt. Dit opgeloste zout verstoort de vorming van de kristalstructuur die ijs moet bevroren blijven. De zoutionen staan in wezen in de weg, waardoor het moeilijker is voor watermoleculen om het stabiele ijsrooster te vormen.
* Praktische toepassingen: Dit principe wordt gebruikt om ijs te smelten op wegen en trottoirs in de winter. Het zout verlaagt het vriespunt van het water en voorkomt dat het opnieuw wordt verteld, zelfs als de temperatuur onder het vriespunt is.
Belangrijke opmerking: Hoewel zout ijs doet, laat het niet noodzakelijkerwijs verdwijnen. Het zout lost eigenlijk op in het water, waardoor een zoute oplossing ontstaat. Deze oplossing kan vervolgens opnieuw bevriezen als de temperatuur laag genoeg daalt, hoewel het vriespunt lager zal zijn dan zuiver water.
 Hoe krijg je vloeibaar ijzer uit vaste stof in chemische reactieformule?
Hoe krijg je vloeibaar ijzer uit vaste stof in chemische reactieformule?  Wat is het verwachte aantal valentie -elektronen voor een groep 3 A -element?
Wat is het verwachte aantal valentie -elektronen voor een groep 3 A -element?  Wat maken verbindingen en atomen moleculen?
Wat maken verbindingen en atomen moleculen?  Welke aanvullende informatie is nodig om de molecuulformule te berekenen op basis van het massapercentage van elk element in een verbinding?
Welke aanvullende informatie is nodig om de molecuulformule te berekenen op basis van het massapercentage van elk element in een verbinding?  Onderzoekers ontwikkelen geheugenapparaten met faseverandering voor krachtiger computergebruik
Onderzoekers ontwikkelen geheugenapparaten met faseverandering voor krachtiger computergebruik
Hoofdlijnen
- Label het axon van het cellichaam?
- Waarom we niet meer verliefd moeten worden op schilferige witte vis
- Zijn de antibiotica lipiden in de natuur?
- Hoe 'winnaar- en verliezerseffecten' de sociale rangorde van dieren en mensen beïnvloeden
- What is the definiton a nascassist?
- Waarom zijn de mentale afbeeldingen die wetenschappers nuttig gebruiken?
- Worden wetenschappelijke ontdekkingen aangestuurd door geweldige individuen of teams?
- Onderzoekers ontdekken dat calcium aardappelplanten kan beschermen tegen bacteriële verwelking
- Wat houdt het cytoplasma en de kern weg van de omringende omgeving?
- Chemici vinden nieuwe manier om de bouwstenen van veel medicijnen te maken

- Moleculaire trillingen verminderen de maximaal haalbare fotospanning in organische zonnecellen
- Wetenschappers hebben een manier voorgesteld om in water oplosbare fullereenverbindingen voor medicijnen te produceren

- Ongebruikelijke suiker van cyanobacteriën werkt als natuurlijk herbicide

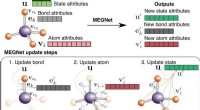
- Ingenieurs gebruiken grafieknetwerken om eigenschappen van moleculen en kristallen nauwkeurig te voorspellen
 Nieuw potentieel voor het volgen van zware stormen
Nieuw potentieel voor het volgen van zware stormen Wat maakt clowns zo griezelig?
Wat maakt clowns zo griezelig?  Aardbeving treft grensgebied Iran-Irak
Aardbeving treft grensgebied Iran-Irak Over het hele spectrum:onderzoekers vinden een manier om de kleur van licht in materiaal van de volgende generatie te stabiliseren
Over het hele spectrum:onderzoekers vinden een manier om de kleur van licht in materiaal van de volgende generatie te stabiliseren Silicon Valley-mysterie:waarom de 'tijd rijp is' voor Eric Schmidt om te vertrekken als voorzitter van Alphabet
Silicon Valley-mysterie:waarom de 'tijd rijp is' voor Eric Schmidt om te vertrekken als voorzitter van Alphabet  Kritische overgangstheorie toont flikkering in het hart vóór atriale fibrillatie
Kritische overgangstheorie toont flikkering in het hart vóór atriale fibrillatie Borium buckyball ontdekt
Borium buckyball ontdekt Wat is micro-biologie?
Wat is micro-biologie?
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

