
Wetenschap
Wat is het verschil tussen een thermodynamisch gunstige en ongunstige reactie?
Thermodynamisch gunstige reacties:
* spontaan: Deze reacties gebeuren meestal op natuurlijke wijze zonder externe input van energie.
* Negatieve Gibbs vrije energieverandering (ΔG <0): Dit geeft aan dat de producten lagere vrije energie hebben dan de reactanten, waardoor de reactie energetisch bergafwaarts wordt.
* Release energie (exotherme): Gunstige reacties geven warmte vaak in de omgeving, maar dit is niet altijd het geval. De verandering in Gibbs Free Energy beschouwt zowel enthalpie (warmte) als entropie (stoornis).
* Voorbeelden:
* Verbranding (verbranding) van brandstof
* Het roesten van ijzer
* Het oplossen van tafelzout in water
Thermodynamisch ongunstige reacties:
* Niet-spontaan: Deze reacties vereisen energie -input om door te gaan.
* Positieve Gibbs vrije energieverandering (ΔG> 0): Dit betekent dat de producten hogere vrije energie hebben dan de reactanten, waardoor energie bergopwaarts moet klimmen.
* Energie -input (endotherm) vereisen: Deze reacties absorberen meestal warmte uit de omgeving.
* Voorbeelden:
* Smeltend ijs (vereist warmte)
* Elektrolyse (water splitsen in waterstof en zuurstof vereist elektrische energie)
* Fotosynthese (planten hebben zonlicht nodig om koolstofdioxide en water om te zetten in glucose)
belangrijke opmerkingen:
* evenwicht: Reacties kunnen een evenwichtstoestand bereiken waar de snelheid van de voorwaartse reactie gelijk is aan de snelheid van de omgekeerde reactie. Dit betekent dat de netto verandering in concentraties van reactanten en producten nul is, hoewel de reactie nog steeds optreedt.
* kinetiek: Thermodynamica vertelt ons of een reactie * mogelijk is * onder gegeven omstandigheden, maar het vertelt ons niet hoe * snel * het zal gebeuren. Kinetiek gaat over reactiesnelheden. Een thermodynamisch gunstige reactie kan erg traag zijn als de activeringsenergiebarrière hoog is.
Samenvattend:
* Gunstige reacties zijn spontaan en geven energie vrij.
* ongunstige reacties vereisen dat energie -input doorgaat.
Laat het me weten als je een diepere duik wilt in een van deze concepten!
 Kun je zilver smelten met een zuurstof- en propaantakker?
Kun je zilver smelten met een zuurstof- en propaantakker?  Wetenschappers gebruiken licht om vetzuren om te zetten in alkanen
Wetenschappers gebruiken licht om vetzuren om te zetten in alkanen Wanneer kleine goudvlokken uit een wateroplossing worden verwijderd door het filteren van de Is dit een fysieke verandering?
Wanneer kleine goudvlokken uit een wateroplossing worden verwijderd door het filteren van de Is dit een fysieke verandering?  Waarom delen atomen de winst of verliezen ze elektronen?
Waarom delen atomen de winst of verliezen ze elektronen?  Onderzoeken hoe korstmossen zichzelf verdedigen tegen giftige metalen en hoge zuurgraad
Onderzoeken hoe korstmossen zichzelf verdedigen tegen giftige metalen en hoge zuurgraad
 Hoe is het zowel een psycologische staat als de fysieke plek?
Hoe is het zowel een psycologische staat als de fysieke plek?  Hoe beïnvloedt Wind Weer Weer?
Hoe beïnvloedt Wind Weer Weer?  Een blik op door het klimaat veroorzaakte schade die zich ontvouwt in Perus Cordillera Blanca
Een blik op door het klimaat veroorzaakte schade die zich ontvouwt in Perus Cordillera Blanca Hoe we de effectiviteit van wereldwijde milieubescherming kunnen vergroten
Hoe we de effectiviteit van wereldwijde milieubescherming kunnen vergroten Onderzoekers ontwikkelen nieuwe verklaring voor destructieve aardbevingstrillingen
Onderzoekers ontwikkelen nieuwe verklaring voor destructieve aardbevingstrillingen
Hoofdlijnen
- Waarom husky’s blauwe ogen hebben
- Waarom zijn nucleische en andere grote biologische moleculen bekend als polymeren omdat?
- Nieuw soort cognitieve robot... een puppy?
- DNA in dunne draadachtige vorm wordt aangeroepen?
- Waar staat G voor in de celcyclus?
- DNA-barcoding van parasitaire wormen:is het koosjer?
- Wat is het proces van blaasjes die hun inhoud buiten de cel vrijgeven?
- Hoe bacteriën hypothiocyaniet onschadelijk maken, een antimicrobieel wapen van het aangeboren immuunsysteem
- Turkije bevrijdt 7, 500 illegaal opgejaagde kikkers de rivier in
- Het bouwen van een betere brandstofcel begint met oppervlaktechemie

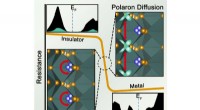
- Team werpt nieuw licht op ontwerp van anorganische materialen voor hersenachtige computers
- Chemici synthetiseren elektroden voor accu's uit koffiedik
- Probe schijnt licht op overactieve immuuncellen om te helpen detecteren, bepaalde vormen van kanker behandelen, auto-immuunziekten

- Lassen met stamcellen voor chirurgische lijmen van de volgende generatie
 Hoe te Reaction Rate van
Hoe te Reaction Rate van  Wat zijn twee ideeën over evolutie die door wetenschappers in de 18e eeuw werden voorgesteld?
Wat zijn twee ideeën over evolutie die door wetenschappers in de 18e eeuw werden voorgesteld?  Hernieuwbare energie kan de natuurlijke wereld redden, maar als we niet voorzichtig waren, het zal ook pijn doen
Hernieuwbare energie kan de natuurlijke wereld redden, maar als we niet voorzichtig waren, het zal ook pijn doen Onderzoeker onderzoekt hoe we de wereldwijde voedselvoorziening veerkrachtiger kunnen maken
Onderzoeker onderzoekt hoe we de wereldwijde voedselvoorziening veerkrachtiger kunnen maken Dit is wat we kunnen doen om de rook van bosbranden uit onze gebouwen te houden
Dit is wat we kunnen doen om de rook van bosbranden uit onze gebouwen te houden  Is een koninkrijksgroep organismen die in hetzelfde gebied leven?
Is een koninkrijksgroep organismen die in hetzelfde gebied leven?  Waarom zou het moeilijker zijn om ziekten bij mensen te behandelen die worden veroorzaakt door leden van de Eucarya dan door bacteriën?
Waarom zou het moeilijker zijn om ziekten bij mensen te behandelen die worden veroorzaakt door leden van de Eucarya dan door bacteriën?  Nieuw centrum om olie en gas te vervangen door duurzame chemie
Nieuw centrum om olie en gas te vervangen door duurzame chemie
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

