
Wetenschap
Een element heeft een zeer laag kookpunt en reactiviteit. Waar op het periodieke tabel is dit het meest waarschijnlijk te vinden?
Dit is waarom:
* Laag kookpunt: Nobele gassen bestaan als enkele atomen, met zeer zwakke interatomische krachten (van der Waals -krachten). Deze zwakke krachten resulteren in lage kookpunten, omdat zeer weinig energie nodig is om ze te overwinnen en ervoor te zorgen dat de atomen zich scheiden in een gasvormige toestand.
* Lage reactiviteit: Nobele gassen hebben een volledige buitenste schaal van elektronen, waardoor ze zeer stabiel en niet -reactief zijn. Ze vormen zelden chemische bindingen met andere elementen.
Voorbeelden: Helium (HE), Neon (NE), Argon (AR), Krypton (KR), Xenon (XE) en Radon (RN) zijn allemaal edelgassen met extreem lage kookpunten en zeer lage reactiviteit.
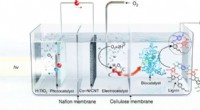
 Water zou de activiteit en selectiviteit van koolstofdioxidereductie kunnen moduleren
Water zou de activiteit en selectiviteit van koolstofdioxidereductie kunnen moduleren Wat is de valentie van koolstof?
Wat is de valentie van koolstof?  Hoeveel valentie-elektronen zullen een element gelukkig of stabiel maken?
Hoeveel valentie-elektronen zullen een element gelukkig of stabiel maken?  Hoe zijn verdamping en koken vergelijkbaar?
Hoe zijn verdamping en koken vergelijkbaar?  Zink-ion hybride condensatoren met ideale anionen in de elektrolyt vertonen extra lange prestaties
Zink-ion hybride condensatoren met ideale anionen in de elektrolyt vertonen extra lange prestaties
 Er is een kaart gemaakt met elf provincies in Californië die het grootste risico lopen op bosbranden
Er is een kaart gemaakt met elf provincies in Californië die het grootste risico lopen op bosbranden  Een viervoudige toename van koolstofdioxide boven Oost-Azië veroorzaakt veranderingen in zowel snelle als langzame wolkenreacties
Een viervoudige toename van koolstofdioxide boven Oost-Azië veroorzaakt veranderingen in zowel snelle als langzame wolkenreacties Verschillen tussen ecocentrisch en biocentrisch
Verschillen tussen ecocentrisch en biocentrisch  Koeler voor delen van Europa, Spanje bestrijdt bosbranden
Koeler voor delen van Europa, Spanje bestrijdt bosbranden Hoe de jacht mensen tot langeafstandslopers heeft gemaakt
Hoe de jacht mensen tot langeafstandslopers heeft gemaakt
Hoofdlijnen
- Op welke manier controleert de samenleving de wetenschap?
- Uit de problemen komen:helpt mobiel DNA?
- Zwakke sociale banden een moordenaar voor mannelijke walvissen
- Nieuwe aanwijzingen over hoe poortwachter voor de celkern werkt
- Wetenschappers ontdekken hoe hormonen hun effecten bereiken
- Wat vertegenwoordigt het nucleaire membraan?
- Hoe kan onderzoekers correcte informatie verkrijgen?
- Kan het vage viraal gaan voor generatie Y?
- Waarom wordt pseudowetenschap niet beschouwd als echte wetenschap?
- Van lab tot plaat:rubberbeton buigt mee naar de residentiële markt

- Apparaat gebouwd voor extreme omgevingen kan de productie van Actinium-225 versnellen

- Biogefunctionaliseerd keramiek voor herstel van schedelbotdefecten - in vivo onderzoek

- Organische/anorganische zwavel kan de sleutel zijn voor veilige oplaadbare lithiumbatterijen

- Nieuw biokatalytisch systeem zet afvalbiomassa om in chemicaliën met toegevoegde waarde
 Italiaanse astronomen inspecteren sterrenstelsel Markarian 509 met ALMA
Italiaanse astronomen inspecteren sterrenstelsel Markarian 509 met ALMA Wat als je de rest van je leven maar één soort voedsel at?
Wat als je de rest van je leven maar één soort voedsel at?  Een nieuw venster om de verborgen kant van het gemagnetiseerde universum te zien
Een nieuw venster om de verborgen kant van het gemagnetiseerde universum te zien Verbetering van de femtoseconde ultrakorte pulslaser
Verbetering van de femtoseconde ultrakorte pulslaser Wat osmose inhoudt. zowel water als zuurstof, maar niet noch noch zuurstof?
Wat osmose inhoudt. zowel water als zuurstof, maar niet noch noch zuurstof?  Ingenieurs ontwikkelen eerst afstembare, op chip gebaseerde vortex microlaser en detector
Ingenieurs ontwikkelen eerst afstembare, op chip gebaseerde vortex microlaser en detector Wordt de hydrosfeer aangedreven door zon of geothermische energie?
Wordt de hydrosfeer aangedreven door zon of geothermische energie?  Hoe luchtvaartmaatschappijen werken
Hoe luchtvaartmaatschappijen werken
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

