
Wetenschap
Wat kan er gebeuren met een ideaal gas en wat geen gas?
ideaal gas
* Definitie: Een ideaal gas is een theoretisch concept waarbij wordt aangenomen dat deeltjes geen volume hebben en geen intermoleculaire krachten hebben.
* Key -kenmerken:
* Geen intermoleculaire krachten: Deeltjes trekken elkaar niet aan of stoten elkaar af.
* Volume verwaarloosbaar deeltjes: Het volume van de deeltjes is onbeduidend in vergelijking met het containervolume.
* Elastische botsingen: Botsingen tussen deeltjes zijn perfect elastisch, wat betekent dat er geen energie verloren gaat.
* volgt de ideale gaswet: Pv =nrt (waarbij p =druk, v =volume, n =mol, r =ideale gasconstante, t =temperatuur).
* wat kan er gebeuren?
* breidt en contracteert vrij: Ideale gassen kunnen voor onbepaalde tijd uitbreiden of contracteren om hun container te vullen.
* volgt de ideale gaswet perfect: De relatie tussen druk, volume, temperatuur en aantal mol wordt altijd nauwkeurig beschreven door de ideale gaswet.
* Constante warmtecapaciteit: De hoeveelheid warmte die nodig is om de temperatuur van een bepaalde hoeveelheid gas te verhogen, is consistent.
* wat kan niet gebeuren?
* condensatie of liquefactie: Ideale gassen condenseren nooit in vloeistoffen, ongeacht hoeveel druk wordt uitgeoefend.
* afwijking van ideaal gedrag: Ideale gassen wijken nooit af van de ideale gaswet, zelfs bij hoge druk of lage temperaturen.
echt gas
* Definitie: Echte gassen zijn de gassen die we in de echte wereld tegenkomen. Ze hebben eindig deeltjesvolume en ervaren intermoleculaire krachten.
* Key -kenmerken:
* intermoleculaire krachten: Deeltjes trekken of afstoten elkaar (bijv. Van der Waals -krachten, waterstofbinding).
* Niet-verwaarloosbaar deeltjesvolume: Het volume van de deeltjes is niet onbeduidend, vooral bij hoge drukken.
* Inelastische botsingen: Sommige energie gaat verloren tijdens botsingen.
* wat kan er gebeuren?
* Condensatie en vloeibaarheid: Echte gassen kunnen condenseren tot vloeistoffen of zelfs stollen bij bepaalde temperaturen en drukken.
* afwijking van ideaal gedrag: Echte gassen wijken af van de ideale gaswet, vooral bij hoge druk of lage temperaturen.
* Variabele warmtecapaciteit: De warmtecapaciteit van een echt gas kan variëren, afhankelijk van de temperatuur en druk.
* wat kan niet gebeuren?
* Volg perfect de ideale gaswet: Echte gassen gehoorzamen niet perfect de ideale gaswet onder alle omstandigheden.
Samenvatting
Ideale gassen zijn een nuttig theoretisch model voor het begrijpen van gasgedrag, maar ze zijn geen perfecte weergave van de realiteit. Echte gassen vertonen meer complex gedrag vanwege de invloed van intermoleculaire krachten en deeltjesvolume.
 Wat is het verschil tussen blauw en rood lakmoespapier?
Wat is het verschil tussen blauw en rood lakmoespapier?  Een gestroomlijnde benadering voor het bepalen van thermische eigenschappen van kristallijne vaste stoffen en legeringen
Een gestroomlijnde benadering voor het bepalen van thermische eigenschappen van kristallijne vaste stoffen en legeringen Hoe fractionele destillatie te verbeteren
Hoe fractionele destillatie te verbeteren Hoeveel elementen zitten er in een atoom?
Hoeveel elementen zitten er in een atoom?  Hoe verhoogt het gebruik van synthetische producten zoals plastic de fossiele brandstoffen?
Hoe verhoogt het gebruik van synthetische producten zoals plastic de fossiele brandstoffen?
 Wat kalmerende van de Hawaii-vulkaan, maar wetenschappers blijven op hun hoede
Wat kalmerende van de Hawaii-vulkaan, maar wetenschappers blijven op hun hoede Betrouwbaar meten van microplastics die vrijkomen bij het wassen
Betrouwbaar meten van microplastics die vrijkomen bij het wassen Door droogte getroffen Kaapstad moet buitenaardse bomen kappen:studie
Door droogte getroffen Kaapstad moet buitenaardse bomen kappen:studie Opwarming van het Russische noordpoolgebied leidt tot groot ijsverlies
Opwarming van het Russische noordpoolgebied leidt tot groot ijsverlies Wat bedoelt de generaal met instinct is niet opgewassen tegen de rede?
Wat bedoelt de generaal met instinct is niet opgewassen tegen de rede?
Hoofdlijnen
- Wat is Mitichondrion?
- Nieuwe techniek helpt onderzoekers bepalen hoe stamcellen differentiëren
- Onderzoekers vinden mechanisme waarmee plantenwortels zuurstofarme grond vermijden
- De aanwijzing zit in de lijm:onderzoek laat zien hoe planten het bij elkaar houden tijdens de groei
- Wat is de meeste verandering in volgorde van basen waarnaar een DNA -molecuul nauwkeurig is verwezen?
- Wat wordt geproduceerd door cellen die zijn geïnfecteerd met virussen?
- Zijn de monomeren van DNA nucleïnezuren?
- Wat zijn de verschillen tussen een CZS en een PNS?
- Wat zijn de 6 Kindoms in de wetenschap?
- Wetenschappers ontsluiten het potentieel van ultradunne 2D-materialen

- Video:hoe Xanax werkt

- Nieuwe methode ontwikkeld om antibioticaresten in voedsel uit dierlijke bronnen te extraheren

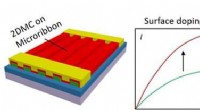
- 2-D moleculaire kristallen die de elektronische eigenschappen van organische halfgeleiders moduleren
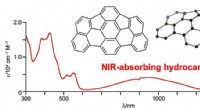
- Moleculaire ontwerpstrategie onthult bijna-infraroodabsorberende koolwaterstof
 Geavanceerde series van robuustere drones leren zichzelf vliegen
Geavanceerde series van robuustere drones leren zichzelf vliegen Ingenieurs 3D-print vormveranderende slimme gel
Ingenieurs 3D-print vormveranderende slimme gel Californië verlengt strenge klimaatbeleidsmaatregelen tot 2030
Californië verlengt strenge klimaatbeleidsmaatregelen tot 2030 Waarom dacht Thomson dat een atoom positieve ladingen moest bevatten?
Waarom dacht Thomson dat een atoom positieve ladingen moest bevatten?  Wat zijn atomen met hetzelfde atoomnummer en chemische eigenschappen in hun puurste vorm?
Wat zijn atomen met hetzelfde atoomnummer en chemische eigenschappen in hun puurste vorm?  Afbeelding:Geologie van de Victoria Vierhoek op Mercurius
Afbeelding:Geologie van de Victoria Vierhoek op Mercurius Waarom worden Richter -schalen schalen genoemd?
Waarom worden Richter -schalen schalen genoemd?  Direct gekoelde elektromotor gemaakt van polymeermaterialen
Direct gekoelde elektromotor gemaakt van polymeermaterialen
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

